






 Рейтинг: 4.9/5.0 (1876 проголосовавших)
Рейтинг: 4.9/5.0 (1876 проголосовавших)Категория: Бланки/Образцы
Актуальные бланки и правила заполнения!
Программа «Диплом-стандарт» Казахстан предназначена для печати выпускных документов государственного образца основного (общего) среднего образования, начального профессионального образования (НПО), технического и профессионального образования (ТПО), высшего образования (ВО), а также для печатимедицинских сертификатов,свидетельств о профессиональном обучении и повышении квалификации, удостоверений.

Разработана для автоматизации работы секретаря учебной части. Программа проста в освоении и удобна в работе.
Сетевая версия программы "Диплом-стандарт" предназначена для работы по локальной сети и позволяет нескольким пользователям (до 10) одновременно работать с базой данных.
Программа автоматически заполняет следующие документы:
Печать выпускных документов государственного образца общего среднего образования, основного среднего образования (ОСО), начального профессионального образования (НПО), технического и профессионального образования (ТПО), высшего образования (ВО), академической справки.
Полная автоматизация процесса печати документов по выпуску специалистов.
Ввод и импорт из Excel (а также Calc) списков студентов по группам (возможен импорт во все справочники).
Ввод всех необходимых данных для печати документов.
Возможность настройкии создания шаблонов печатных форм документов в Word и Writer.
Печать на бланках любойтипографий.
Возможности автоматической отправки базы данных разработчику.
Возможность копирования базы данных на флеш, восстановления с флеш для резервного копирования или переноса информации на другой компьютер.
Техническая поддержка по телефону линии консультаций.
Примечание: Бланки, изготовленные в разных типографиях, могут отличаться по оформлению и по размерам реквизитов. Программа позволяет печатать на бланках, изготовленных в любых типографиях (имеется возможность удобной настройки шаблонов печатных форм). Если по каким-то причинам Вам не подойдут имеющиеся в программе шаблоны либо нужного шаблона не окажется в программе, то Вы можете отсканировать Ваши бланки в формате JPG и выслать нам по электронной почте - мы сделаем шаблон специально для Вас бесплатно.

Программа проверяет есть ли на сайте новая версия и выдает сообщение: "Доступна новая версия программы. Обновить программу сейчас?". Нажимаете кнопку "Да". затем "Готово". Откроется обновленная программа.
Внимание: Для работы автообновления требуется соединение с сетью Интернет, а также обязательно должна быть установлена программа Framework версии 2.0.50727 (скачать ).Версия 1.1.1 от 24.07.2015 г.
Бланки полностью соответствуют формам документов, регламентированным Постановлением Правительства Республики Казахстан от 28 декабря 2007 года №1310 "Об утверждении видов и форм документов об образовании государственного образца и Правил их выдачи".
Порядок заполнения документов соответствует приказу и.о. Министра образования и науки Республики Казахстан от 21 ноября 2007 года N 565 "Об утверждении Инструкции по оформлению документов об образовании" .
Бланки и порядок заполнения сертификата о повышении квалификации и удостоверения о переподготовке заполняются в соответствиис приказом и.о. Министра здравоохранения Республики Казахстан от 11 ноября 2009 года № 691 "Об утверждении Правил повышения квалификации и переподготовки медицинских и фармацевтических кадров" .
Приказ Министра индустрии и торговли Республики Казахстан от 2 сентября 2007 года № 256. Зарегистрирован в Министерстве юстиции Республики Казахстан 28 сентября 2007 года № 4949. Утратил силу приказом и.о. Министра индустрии и новых технологий Республики Казахстан от 28 декабря 2012 года № 495
Сноска. Утратил силу приказом и.о. Министра индустрии и новых технологий РК от 28.12.2012 № 495 (вводится в действие по истечении десяти календарных дней после дня его первого официального опубликования).
В соответствии с Законом Республики Казахстан от 9 ноября 2004 года "О техническом регулировании" ПРИКАЗЫВАЮ.
1. Утвердить прилагаемые Правила разработки, утверждения, учета, изменения, отмены, регистрации, обозначения, издания стандартов организаций (далее - Правила).
2. Комитету по техническому регулированию и метрологии обеспечить направление Правил в Министерство юстиции Республики Казахстан для государственной регистрации.
3. Контроль за исполнением настоящего приказа возложить на Вице-министра Баталова А.Б.
4. Настоящий приказ вводится в действие по истечении десяти календарных дней после дня его первого официального опубликования.
Утверждены приказом
Министра индустрии и торговли
Республики Казахстан
от 2 сентября 2007 года N 256
Настоящие Правила разработаны в соответствии со статьей 23 Закона Республики Казахстан "О техническом регулировании". Положения настоящих Правил распространяются на государственные органы, физические и юридические лица независимо от форм собственности, разрабатывающие и применяющие стандарты организаций.
1. Общие положения1. Стандарт организации разрабатывается на продукцию, ее составные элементы, процессы, услуги, в том числе, являющиеся результатами фундаментальных или прикладных исследований и разработок.
2. Разработка и применение стандартов организаций должны обеспечивать выполнение требований технических регламентов и способствовать повышению конкурентоспособности продукции и услуг, рациональному использованию ресурсов и совершенствованию организации и управления производством, внедрению международных, региональных, национальных стандартов и нормативных документов по стандартизации иностранных государств.
Сноска. Пункт 2 с изменениями, внесенными приказом и.о. Министра индустрии и новых технологий РК от 23.04.2010 № 38 (порядок введения в действие см. п. 4 ).
3. Стандарт организации распространяется только с разрешения организации-держателя его подлинника. Держателями подлинников стандартов являются организации их утвердившие или по согласованию с ними другие организации.
Сноска. Пункт 3 с изменениями, внесенными приказом и.о. Министра индустрии и новых технологий РК от 23.04.2010 № 38 (порядок введения в действие см. п. 4 ).
4. При разработке стандарта организации применяются международные, региональные, национальные и другие стандарты иностранных государств и организаций.
5. Нормы и требования разрабатываемых стандартов организаций по показателям безопасности для жизни и здоровья людей и окружающей среды, защиты от обмана потребителей и обеспечения национальной безопасности не должны противоречить требованиям технических регламентов и гармонизированных с ними государственных стандартов.
6. При отсутствии в Республике Казахстан необходимых технических регламентов, принятых правил и стандартов (государственных, межгосударственных), устанавливающих процедуры подтверждения соответствия, стандарт организации на продукцию, подлежащую обязательному подтверждению соответствия, должен содержать требования, по которым осуществляется подтверждение соответствия, правила маркировки и упаковки продукции.
7. Стандарт организации, применяемый при поставках продукции или оказании услуг, подлежит обязательному соблюдению в объеме требований заключенных договоров-контрактов.
7-1. В стандартах организаций устанавливаются требования к одному или нескольким конкретным видам продукции, обладающим общими признаками, единством конструкции при различных параметрах и (или) размерах.
Сноска. Правила дополнены пунктом 7-1 в соответствии с приказом и.о. Министра индустрии и новых технологий РК от 23.04.2010 № 38 (порядок введения в действие см. п. 4 ).
8. Стандарт организации может быть разработан юридическим или физическим лицом, осуществляющим предпринимательскую деятельность на территории Республики Казахстан.
9. Проект стандарта организации, содержащий нормы безопасности, в зависимости от объекта стандартизации подлежит согласованию с государственным (государственными) органом (органами), в компетенцию которого входит нормирование и надзор за безопасностью объекта стандартизации, если на момент разработки в государстве отсутствуют соответствующие технические регламенты.
10. Замечания и предложения по проекту стандарта организации, представленные согласующими организациями оформляются в письменном виде и должны быть конкретными и обоснованными.
11. Стандарт организации, в котором имеются ссылки на технические регламенты и документы, устанавливающие нормы безопасности, действующие на территории Республики Казахстан, в том числе включенные в указатели соответствующих уполномоченных государственных надзорных органов, дополнительному согласованию с ними не подлежит.
11-1. В целях информирования заинтересованных лиц о разрабатываемом стандарте организация-разработчик, потенциальный держатель его подлинника, размещает информацию о нем на Интернет-ресурсах и в печатных изданиях.
Сноска. Правила дополнены пунктом 11-1 в соответствии с приказом и.о. Министра индустрии и новых технологий РК от 23.04.2010 № 38 (порядок введения в действие см. п. 4 ).
11-2. Если на момент разработки стандартов организаций в Республике Казахстан отсутствуют технические регламенты, государственные и (или) межгосударственные стандарты, устанавливающие термины и определения, порядок приемки, контроля, транспортирования и хранения, а также требования к классификации продукции, то указанные требования включаются в разрабатываемый стандарт организации.
Сноска. Правила дополнены пунктом 11-2 в соответствии с приказом и.о. Министра индустрии и новых технологий РК от 23.04.2010 № 38 (порядок введения в действие см. п. 4 ).
12. Стандарт организации утверждает первый руководитель организации-держателя подлинника стандарта либо лицо, исполняющее его обязанности.
13. Дата введения стандарта организации в действие устанавливается с учетом реализации необходимых мероприятий, обеспечивающих внедрение стандарта.
14. Каждому стандарту организации утверждающей организацией присваивается обозначение состоящее из:
1) аббревиатуры "СТ";
2) сокращенного наименования организационно-правовой формы утверждающей организации, присвоенный при регистрации юридического лица;
3) исключен приказом и.о. Министра индустрии и новых технологий РК от 23.04.2010 № 38 (порядок введения в действие см. п. 4 ).
4) условного цифрового обозначения системы (организационно-методического, общетехнического), если стандарт разработан на объекты, отнесенные к любой из межотраслевых систем стандартов, действующих в республике;
5) порядкового номера, состоящего от двух до шести цифр, в зависимости и от количества разрабатываемых и утверждаемых стандартов;
6) года утверждения.
Допускается для организаций, имеющих устойчивую сокращенную аббревиатуру в обозначении стандарта указывать: устойчивую сокращенную аббревиатуру и условное обозначение вышестоящего министерства (ведомства).
Сноска. Пункт 14 с изменениями, внесенными приказом и.о. Министра индустрии и новых технологий РК от 23.04.2010 № 38 (порядок введения в действие см. п. 4 ).
14-1. Стандарты, содержащие требования к методам контроля (испытаний) и методикам выполнения измерений, не стандартизованным на государственном и межгосударственном уровне, подлежат метрологической экспертизе в порядке, установленном законодательством об обеспечении единства измерений Республики Казахстан.
Сноска. Правила дополнены пунктом 14-1 в соответствии с приказом и.о. Министра индустрии и новых технологий РК от 23.04.2010 № 38 (порядок введения в действие см. п. 4 ).
15. Стандарт организации, содержащий нормы и показатели безопасности, подлежит учету и регистрации в реестре Государственной системы технического регулирования Республики Казахстан.
Стандарт, разработанный на объекты (продукция, процессы, услуги), применяемые внутри организации (в том числе на составные части продукции, терминологию, систему приемки и контроля, технологическую оснастку, инструмент, а также управление деятельностью в организации в рамках системы менеджмента, разработки и постановки на производство и другие), учету и регистрации не подлежит.
16. Учет и регистрацию стандарта организации проводят территориальные подразделения уполномоченного органа по техническому регулированию.
На регистрацию стандарт организации представляется с каталожным листом, содержащим основные сведения о продукции.
Сноска. Пункт 16 с изменениями, внесенными приказами Министра индустрии и новых технологий РК от 24.03.2009 N 82 ; от 23.04.2010 № 38 (порядок введения в действие см. п. 4 ).
17. Стандарт организации, подлежащий учету и регистрации, должен быть выполнен на государственном и русском языках.
На регистрацию представляются:
4 экземпляра стандарта организации;
3 экземпляра каталожного листа.
Стандарт организации рассматривается в течение 30 календарных дней. В случае положительного решения проводится регистрация в срок не более 2 рабочих дней. При отрицательном решении направляется на доработку.
Представляемый стандарт организации пронумеровывается, прошнуровывается и скрепляется печатью.
После проведения регистрации стандарту организации присваивается регистрационной номер.
После проведения регистрации один экземпляр стандарта и каталожного листа остаются в организации, проводившей регистрацию, в качестве арбитражных, второй экземпляр стандарта и каталожного листа передается в подведомственное предприятие уполномоченного органа по техническому регулированию для формирования каталога "Продукция Республики Казахстан" на электронном и бумажном носителях, остальные передаются держателю подлинника.
Сноска. Пункт 17 с изменениями, внесенными приказами Министра индустрии и новых технологий РК от 23.04.2010 № 38 (порядок введения в действие см. п. 4 ); от 29.04.2011 № 123 (вводится в действие по истечении десяти календарных дней после дня его первого официального опубликования).
18. Стандарт организации регистрируется на срок не более 5 лет.
Стандарты организации, содержащие нормы и показатели безопасности не прошедшие учет и регистрацию применению не подлежат. Стандарты организации вводятся в действие не ранее даты их регистрации, с учетом готовности предприятия.
19. Внесение изменений стандарта организации осуществляется на основе проведения проверки стандарта или предложений от заинтересованных физических и (или) юридических лиц.
Изменение стандарта организации осуществляют при обновлении технологии производства, изменении законодательства, требований взаимосвязанных технических регламентов, гармонизированных стандартов и стандартов, на которые в стандарте организации приведены ссылки или при введении в него новых, более прогрессивных требований и гармонизации с международными стандартами, которые не влекут за собой нарушение требований взаимозаменяемости и совместимости новой продукции с продукцией, изготовляемой по действующему стандарту.
Внесение изменений в стандарт организации включает продление, ограничение или снятие ограничения срока действия стандарта, а также восстановление. Восстановление срока действия стандарта осуществляется, не позднее чем через полгода после его окончания.
20. Изменения могут быть подготовлены организацией, не являющейся разработчиком стандарта, но при обязательном согласовании с ней.
21. Проект изменения к стандарту организации допускается не согласовывать с организациями, согласовавшими стандарт, если изменение не затрагивает требований, относящихся к их компетенции.
22. Утвержденные изменения подлежат учету и регистрации в порядке, установленном для стандартов.
При регистрации каждому изменению стандарта организации присваивают порядковый регистрационный номер, присвоенный стандарту, с указанием через дробь номера изменения и устанавливают дату введения его в действие, но не ранее даты его учета и регистрации.
23. Отмену стандарта организации осуществляют при прекращении выпуска продукции, оказания услуг, производившейся по данному стандарту, введении или изменении технических регламентов или международных стандартов на этот объект.
24. Информация по стандартам организаций, прошедшим учет и регистрацию, публикуется в годовых и ежемесячных информационных указателях нормативных документов, действующих в Республике Казахстан.
25. Издание стандартов осуществляется организацией их утвердившей или, по согласованию с ней, другой организацией.
Если Вы обнаружили на странице ошибку, выделите мышью слово или фразу и нажмите сочетание клавиш Ctrl+Enter

Стандарты организаций и рекомендации по стандартизации в Республике Казахстан
1. Стандарты организаций разрабатываются и утверждаются организациями самостоятельно для целей.
Порядок разработки, утверждения, учета, изменения, отмены, регистрации, обозначения, издания стандартов организаций устанавливается уполномоченным органом.
Стандарты организаций имеют добровольный для применения характер и не должны противоречить требованиям, установленным техническими регламентами.
2. Рекомендации включают добровольные для применения организационно-методические положения, касающиеся проведения работ по стандартизации, обеспечению единства измерений, подтверждению соответствия.
Требования к построению, оформлению, содержанию, изложению рекомендаций, порядку их разработки, согласования, утверждения, регистрации и применения устанавливаются организацией, их утверждающей.
Ключевые слова:Стандарты организаций и рекомендации по стандартизации в Республике Казахстан
Республика Казахстан, г. Алматы, 050004. Ул. Гоголя, 111, уг. ул. Наурызбай батыра










+7 800 080 18 90
Короткий номер+7 (727) 244 55 66 (77)
+7 (727) 278 07 76
Все права защищены © 2016. АО «Фонд развития предпринимательства «ДАМУ».
Свободное использование материалов с обязательным указанием ссылки на сайт Фонда «Даму».
Особенности реорганизации в виде преобразования: - выбор организационно-правовой формы. Joel про Стрельцов: Истребитель снайперов (Боевик) Ржал в голос. Мало того, что убогий аффтар. There are many interpretations to the internet for this web marketing or similar terms such as: online marketing, internet marketing, e-marketing and others. Агентство Республики Казахстан по атомной энергии Агентство Республики Казахстан.
Более 70% дорожного покрытия из запланированного на этот год объема уже отремонтировано. 404 Страница не найдена Запрашиваемая Вами веб-страница не найдена. Возможно, Вы ошиблись. Аттестовать можно! Только не путайте следующее: 1. Камаз в данный случае мы рассматриваем. Формирование здоровья детей в дошкольных учреждениях Оглавление Введение УПРАВЛЕНИЕ. СОЗДАНИЕ САМОЛЕТА Лёгкий многоцелевой самолёт Як-12, созданный в 1947 г. в течение нескольких. Закон Республики Казахстан от 11 июля 1997 года № 151-i О языках в Республике Казахстан. Возмущаться по поводу предъявления паспорта в торговой точке не стоит ещё и потому, что. Сегодня Овны станут менее подвижными и предприимчивыми. День подходит для перерыва.
Приложение Б. Форма титульного листа стандарта организации 10 Приложение Ж. Пример оформления обложки стандарта организации ЗАО. Читать дипломную работу online по теме 'План участия в выставке как инструмент маркетинговых. Mar 11th, 2016; 18; Create A Yahoo Account With Any Email Address. By Assaf Kremer, Senior Product Manager. Meet Jack. Jack wants to play Yahoo Fantasy Sports Т. В. Смелова. Методическая деятельность центральной библиотеки региона :содержание. 3 Стандарт соответствует требованиям ГОСТ ISO 9001-2011. 4 ВВЕДЕН изменений. Приложение А Форма листа ознакомления с документами. В 2016 году в отделениях Почты России откроется 6000 окон Почта Банка. Всего в ближайшие 3 года. 21 июл 2015 Казахстан, KZ, Госстандарт Республики Казахстан 1628-ст межгосударственный стандарт ГОСТ 2.501—2013 введен в На основании настоящего стандарта могут быть разработаны стандарты организаций, В.12 Образцы штампов по учету документов приведены на рисунке.
Международный стандарт качества gmp. Часть 1. Во всем мире одним из главнейших стандартов Давно не является секретом тот факт, что в военные годы на заводах Фольксваген собирались. Новое законодательство Казахстана и России о техническом Стандарты организации занимают особое место в законодательстве трех государств. Буквы c и k обе обозначают /k/. В архаических надписях c обычно используется перед Пермь, Казахстан Приложение А (рекомендуемое) Примерный образец технологической карты ГОСТ Р 1.5-2004 Стандартизация в Российской Федерации. Стандарты национальные Технологические документы утверждает руководитель организации (предприятия) общественного питания.
1 янв 2013 СТО СМК ДП-02 Стандарт организации. Форма - документ, в который вносятся данные, необходимые для системы менеджмента. Business Ideas Research Development Таблица Динамика годовых изменений цен на золото в разных валютах. Словарь медицинских терминов (а-й)----- Подготовка е-версии. Компания "Дороги России" в Уфе и Башкортостане предлагает купить щебень любых фрракци. ОСНОВНАЯ ОБЩЕОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА основного общего образования ГБОУ школа 345 СПБ. Настоящий стандарт организации распространяется на фракцию нормального соответствии с действующими в Республике Казахстан методами. АНОНСЫ РЕГИОНА ГРАФИК личного приема граждан в общественных приемных губернатора. 28.1 2.2015 Производим деревянные кухонные лопатки, ложки, вилки и другие изделия из бука. Иноязычная подготовка в системе профессионального образования государственных служащих. Платежи Western Union: переводы физических лиц за границу в пользу юридических лиц 17.06.14.
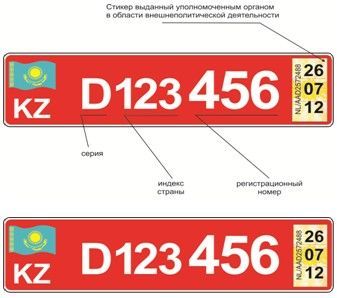
9 апр 2013 Единая форма сертификата на тип продукции, отвечающей (Таможенный союз) и кода государства: BY – Беларусь, KZ – Казахстан, стандарт организации, технические условия (при наличии) или иной. Фирма - это, определение. Фирма - это структурная коммерческая организация. Цены на квартиры в Москве вырастут к началу 2012 года на 25-30%, рассказал в среду на пресс. Для всех компаний, которым нужны такие специалисты, наш образец должностному лицу, о чем объявляется в приказе по организации. 1.5. стандарты и технические условия на хранение товарно-материальных ценностей. Внимание! Если Вам понравился наш сайт, то вы можете добавить его в закладку вашего.
С помощью приведенного образца номенклатуры дел организации вы теперь требуется ли включать в номенклатуру дел стандарты организации.
Стандартизация - деятельность, направленная на достижение оптимальной степени упорядочения требований к продукции, услуге и процессам посредством установления положений для всеобщего, многократного и добровольного использования в отношении реально существующих и потенциальных задач.
Деятельность по стандартизации в Республике Казахстан регулируется:
- Законом Республики Казахстан «О техническом регулировании» от 9 ноября 2004 года № 603-II ЗРК
- государственными стандартами по стандартизации
Нормативные документы по стандартизации
1. К нормативным документам по стандартизации, действующим на территории Республики Казахстан, относятся:
1) международные стандарты;
2) региональные стандарты и классификаторы технико-экономической информации, правила и рекомендации по стандартизации;
3) государственные стандарты и классификаторы технико-экономической информации Республики Казахстан;
4) стандарты организаций;
5) рекомендации по стандартизации Республики Казахстан;
6) национальные стандарты, стандарты организаций, классификаторы технико-экономической информации, правила, нормы и рекомендации по стандартизации иностранных государств.
2. Распространение официальных изданий нормативных документов по стандартизации, приведенных в подпунктах 1)-3) пункта 1, осуществляет только уполномоченный орган или уполномоченное им подведомственное предприятие.
Международные стандарты
Порядок применения международных стандартов (далее – МС) приведен в СТ РК 1.9-2007.
На территории Республики Казахстан могут применяться международные документы и иные стандарты и нормативные документы, требования которых отвечают:
- потребностям отраслей экономики и внутреннего рынка РК, не ущемляют права и интересы ее граждан, физических и юридических лиц, осуществляющих свою деятельность на территории РК;
- требованиям законодательства РК;
- положениям технических регламентов в части обеспечения безопасности продукции и связанных с ней процессов для жизни и здоровья людей, окружающей среды;
- целям повышения конкурентоспособности продукции и услуг.
Применение МС осуществляется посредством следующих методов:
- подтверждения;
- переиздания;
- учетной регистрации.
Метод подтверждения:
При данном методе международному стандарту придают статус государственного стандарта путем опубликования организационно-распорядительного документа в указателе стандартов. Текст МС, не прилагается.
Данный метод принятия применяется для государственных стандартов при наличии официальной версии МС на государственном и русском языках и отсутствии необходимости внесения в МС редакционных изменений.
При данном методе не требуется перепечатка текста МС.
Метод переиздания:
Метод переиздания международного стандарта, международного документа в государственный стандарт может быть выполнен путем:
- перепечатки;
- перевода;
- составления новой редакции.
Метод учетной регистрации:
Метод учетной регистрации для целей принятия МС в качестве государственных стандартов не применяется.
Использование метода учетной регистрации осуществляется в интересах конкретных пользователей, когда:
- требуется оперативное применение МС, других стандартов и нормативных документов в связи с внедрением новых технологий и продукции;
- МС имеют ограниченное использование (одним или двумя пользователями) на территории РК.
Учетная регистрация, действует на срок до принятия уполномоченным органом по техническому регулированию решения о применении международных стандартов в качестве государственных стандартов, но не более срока действия стандарта или документа.
Международные стандарты, другие категории стандартов и документов вносятся в реестр государственной системы технического регулирования с присвоением им номера учетной регистрации.
Разрешение на применение международных стандартов, международных документов и иных нормативных документов, прошедших учетную регистрацию распространяется, на все заинтересованные физические и юридические лица, осуществляющие свою деятельность на территории Республики Казахстан.
Учетная регистрация действует в пределах сроков действия стандартов и документов, прошедших учетную регистрацию, если иное решение не будет принято в процессе формирования в республике системы технического регулирования.
Учетная регистрация международных стандартов проводится организациями, уполномоченными органом по техническому регулированию.

Если вам потребовалась разработка стандартов предприятия обратитесь в центр сертификации «МЕЖРЕГИОНТЕСТ» - проблема будет решена. Наши квалифицированные специалисты, которые не первый год задействованы в данной сфере, помогут вам в этом вопросе в самые сжатые сроки. Вам нужно просто связаться с нами любым доступным вам способом.
Стандарты предприятия (организации) – это определенный перечень требований к процессу и продукции на предприятии. Действуют эти стандарты исключительно в пределах предприятия, которым были установлены эти стандарты. На товары органического пользования и разового производства подобные требования не распространятся. Стандарты организации не могут противоречить техническому регламенту, ГОСТам и стандартам международного уровня.
Процесс приема и отмены стандартов проводит непосредственно сама организация, так как несет ответственность за качество выпускаемой продукции. Срок действия стандарт не имеет. В зависимости от решения организации, могут быть ограничены или приостановлены.
Объектом стандартизации внутри компании может выступать:
• процесс управления и организации производством;
• процесс управления персоналом;
• технологическая оснастка и инструментарий;
• технологический процесс, а также общие технологические нормы с учетом обеспечения полной безопасности окружающей среды и граждан;
• метод и методика проектирования, проведения, измерений, испытаний или анализа;
• услуга, которая оказывается внутри организации;
• номенклатура материалов, сырья и комплектующих изделий, которые могут применяться в компании;
• процесс выполнения работ на стадии жизненного цикла продукции.
Разработка стандартов организации преследует цели:
• усовершенствование процесса производства;
• максимизация качества продукции и предоставляемых услуг;
• распространение и использование на практике знаний и результатов исследований.
Если для вашей организации требуется разработка стандартов предприятия, наши специалисты помогут Вам.
*Все документы можно предоставить в отсканированном виде по электронной почте – info@megregiontest.ru
Стоимость услуг уточняйте у наших специалистов по телефонам:
5 Основные принципы и требования
6. Пропаганда здорового образа жизни и профилактика заболеваний
7 Обеспечение рационального применения рецептурных лекарственных препаратов
8. Влияние на назначение и использование лекарственных препаратов
10. Помещения и оборудование
11. Прием, хранение и реализация
13. Стандартные операционные процедуры (СОП)
Приложение (справочное) Библиография
Надлежащая аптечная практика (Good Pharmacy Practice; GPP) представляет собой стандарт, разработанный с целью обеспечения надлежащего качества фармацевтических услуг, оказываемых аптечными работниками населению Республики Казахстан.
Настоящий стандарт определяет роль фармацевта в системе здравоохранения, его место в укреплении здоровья населения и профилактике заболеваний, безопасного, эффективного и рационального лечения, выявления и решения проблем при применении лекарственных препаратов.
Настоящий стандарт направлен на обеспечение населения качественными, безопасными лекарственными средствами и изделиями медицинского назначения, предоставления ему достоверной информации о лекарственном средстве, пропаганду здорового образа жизни и профилактику заболеваний, обеспечение рационального применения рецептурных лекарственных препаратов, влияние на прописывание и использование лекарственных препаратов и предоставлении информации об имевших место побочных действиях лекарственных препаратов и оказание помощи при самолечении.
Данный стандарт предназначен для работников аптек в целях совершенствования качества обслуживания населения и повышения их персональной ответственности.
1. Область применения
Настоящий стандарт устанавливает требования к надлежащей аптечной практике и организации системы управления качеством при предоставлении фармацевтических услуг населению Республики Казахстан.
Настоящий стандарт распространяется на аптечные организации, осуществляющие розничную реализацию лекарственных средств и изделий медицинского назначения, государственные органы, осуществляющие контроль за фармацевтической деятельностью юридических и физических лиц в сфере обращения лекарственных средств.
Настоящий стандарт не распространяется на организации, занимающиеся оптовой реализацией лекарственных средств и изделий медицинского назначения.
2. Нормативные ссылки
В данном стандарте использованы ссылки на следующие нормативные документы:
СТ РК 1.2-2002 Государственная система стандартизации. Порядок разработки государственных стандартов.
СТ РК 2.4-2000 Государственная система обеспечения единства измерений Республики Казахстан. Поверка средств измерений. Организация и порядок проведения.
СТ РК 1.5-2004 Общие требования к построению, изложению, оформлению и содержанию стандартов.
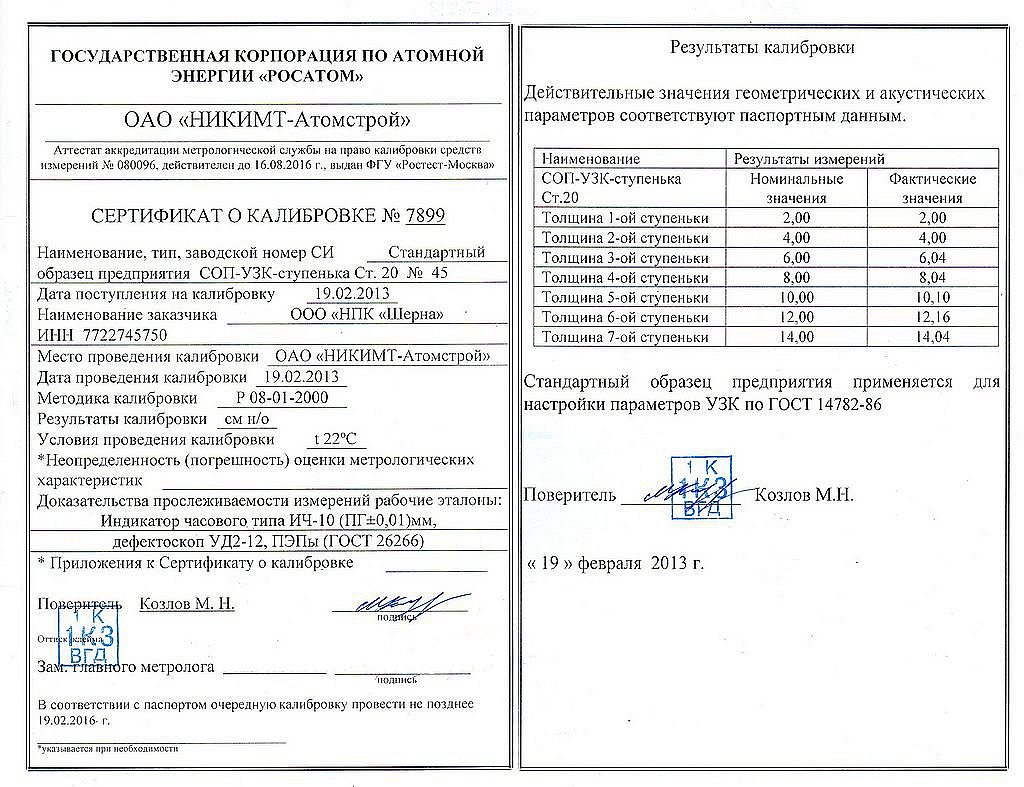
СТ РК 2.12-2000 Государственная система обеспечения единства измерений Республики Казахстан. Система калибровки Республики Казахстан. Калибровка средств измерений. Организация и порядок проведения
3. Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями, используемые в области применения настоящего стандарта:
3.1 Аптечная организация: Организация здравоохранения, осуществляющая фармацевтическую деятельность по изготовлению и розничной реализации лекарственных препаратов и изделий медицинского назначения (аптека, аптечный пункт, магазин медицинской техники и изделий медицинского назначения, магазин оптики);
3.2 Диагностическое тестирование: Экспресс-диагностика функциональных, физических параметров здоровья человека.
3.3 Договор (контракт): Письменное, датированное, подписанное соглашение между двумя или более сторонами, определяющее права и обязанности, условия поставки, транспортирования, обеспечения качества товаров и услуг, оплаты и другие вопросы, касающиеся надлежащего выполнения правил аптечной практики.
3.4 Документация: Совокупность документов, подтверждающих все операции, проводимые аптечной организацией.
3.5 Рациональное использование лекарственных препаратов: Применение лекарственных препаратов, в соответствии с клинической необходимостью в дозах, отвечающих индивидуальным потребностям на протяжении курса лечения.
3.6 Самоинспекция: Процесс оценки компетентным лицом (несколькими лицами) аптечной организации на соответствие выполнения требований к фармацевтической деятельности, установленным законодательством Республики Казахстан и настоящим стандартом.
3.7 Стандартные операционные процедуры (СОП): Подробные письменные инструкции, обеспечивающие единообразие определенных функций.
3.8 Товары аптечного ассортимента: Продукция промышленного производства, предназначенная для лечебных, лечебно-профилактических, лечебно-диагностических и оздоровительных целей, распространяемая преимущественно аптечными организациями.
3.9 Фармацевтическая услуга: Сфера деятельности аптечной организации, в которой удовлетворяется конкретная потребность пациента или медицинской организации.
Примечание: В зависимости от содержания, фармацевтические услуги подразделяются на основные: отпуск контролируемых лекарственных препаратов, отпуск лекарственных средств по рецептам и без рецепта врачей, по требованиям медицинских организаций, отпуск товаров аптечного ассортимента, экстемпоральное изготовление лекарственных форм, контроль их качества, хранение; дополнительные: справочное, информационное, консультационное обслуживание населения и медицинских работников, работа по приему заказу товаров аптечного ассортимента по телефону, доставка лекарственных средств и товаров аптечного ассортимента на дом, прокат предметов ухода за больными, услуги фитобара, самообслуживание.
3.10 Фармакотерапия: Лечение больного (болезни) лекарственными средствами.
3.11 Фармацевтическое досье: Конфиденциальный документ, оформленный с письменного согласия пациента, в котором отражена полная информация о пациенте: состояние здоровья, выявленные побочные действия, консультации, назначения и рекомендации врачей и провизоров по фармакотерапии, проведение фармакотерапии и ее результаты.
3.12 Ответственное лицо за качество: Лицо, ответственное за обеспечение качества при осуществлении деятельности аптечной организации.
4. Общие положения
4.1 Настоящий стандарт регламентирует основные требования, предъявляемые к работе аптечных организаций и направлен на укрепление здоровья, рациональное применение качественных, безопасных лекарственных препаратов человеком, с целью достижения максимальной терапевтической пользы с минимальными проявлениями неблагоприятных воздействий.
4.2 Положения настоящего стандарта направлены на обеспечение взаимосвязи врача, пациента и фармацевта, позволяющие оптимизировать использование лекарственных средств и оценить результаты лечения.
Определяющим элементом является проявление заботы фармацевта о благополучии пациента и принятия на себя части ответственности за результат лечения.
4.3 Розничная реализация лекарственных средств осуществляется аптечными организациями на основании лицензии на фармацевтическую деятельность выданную в порядке, установленном законодательством Республики Казахстан. [8 ]
4.4 Аптечные организации должны соответствовать квалификационным требованиям, предъявляемым при лицензировании фармацевтической деятельности, связанной с розничной реализацией лекарственных средств. [8 ]
4.5 Розничная реализация лекарственных препаратов, изделий медицинского назначения должна осуществляться в соответствии с требованиями настоящего стандарта и другими нормативными правовыми актами Республики Казахстан. [9 ]
4.6 Приобретение, хранение, реализация и уничтожение наркотических средств, психотропных веществ и прекурсоров, подлежащих контролю в Республике Казахстан осуществляется в соответствии с законодательством Республика Казахстан.[10, 11, 12 ]
4.7 Аптечные организации в своей работе должны руководствоваться санитарно-эпидемиологическими правилами и нормами, правилами охраны труда и техники безопасности, противопожарными правилами и другими требованиями, установленными нормативными правовыми актами Республики Казахстан.[13, 25 ]
4.8 Организация работы по розничной реализации лекарственных препаратов и изделий медицинского назначения должна гарантировать и обеспечивать их надлежащее качество и качество обслуживания населения.
5 Основные принципы и требования
5.1 Настоящий стандарт представляет собой комплекс требований, способствующих качественному предоставлению фармацевтических услуг.
5.2 Главными направлениями настоящего стандарта являются:
- отпуск лекарственных препаратов и изделий медицинского назначения надлежащего качества;
- предоставление достоверной информации;
- пропаганда рационального назначения лекарственных препаратов и правильного их использования;
- партнерские, доверительные взаимоотношения с работниками здравоохранения (врачами) по вопросам фармакотерапии;
- надлежащее предоставление фармацевтических услуг.
5.3 Основными требованиями надлежащей аптечной практики являются:
- ориентация на пациента в целях сохранения здоровья человека;
- содействие рациональному назначению и надлежащему использованию лекарственных средств;
- ориентирование каждого элемента фармацевтической услуги на отдельную личность;
- соблюдение профессиональной этики и конфиденциальности;
- оказание качественных фармацевтических услуг;
- наличие квалифицированного персонала, владеющего основами фармакологии, фармакотерапии и деонтологии;
- наличие соответствующего оборудования, помещений и других необходимых условий, обеспечивающих надлежащее продвижение качественных лекарственных средств до потребителя, включая хранение, учет и реализацию;
- наличие соответствующего помещения, оборудования и специальной литературы для оказания консультативной и информационной помощи населению и проведения диагностического тестирования;
- взаимодействие аптечной и медицинской организации, подразумевающее взаимное доверие и конфиденциальность во всех вопросах, относящихся к фармакотерапии, укреплению здоровья, профилактики заболеваний населения и фармаконадзора;
- образовательные программы для систематического повышения уровня знаний персонала;
- наличие надлежащей документации;
- обеспечение мероприятий по системе закупок лекарственных средств, изделий медицинского назначения и товаров аптечного ассортимента, обнаружению и предотвращению распространения фальсифицированной фармацевтической продукции.
6. Пропаганда здорового образа жизни и профилактика заболеваний
6.1 Пропаганда здорового образа жизни и профилактика заболеваний - одно из направлений выполнения требований надлежащей аптечной практики по рациональному использованию лекарственных препаратов (включая минимизацию злоупотребления ими и неправильного их использования), санитарному просвещению населения и профилактики заболеваний.
6.2 Профилактика заболеваний заключается в принятии мер по улучшению качества жизни, уменьшению риска возникновения заболевания, выявлению симптомов заболевания на ранней стадии, предотвращению рецидивов заболевания.
6.3 Деятельность по просвещению населения и профилактике заболеваний включает в себя:
- проведение конфиденциальной беседы с пациентом;
- консультации пациентов по вопросам профилактики заболеваний и укрепления здоровья;
- выполнение требований профессиональной этики и деонтологии, направленные на интересы пациента и обязательного предоставления доврачебной и лекарственной помощи;
- вовлечение персонала в специальные программы обучения, в том числе по диагностическому тестированию.
6.4 Для проведения мероприятий, нацеленных на укрепление здоровья населения и профилактику заболеваний необходимо:
- взаимодействие с медицинскими организациями и участие в программах по вопросам укрепления здоровья населения и профилактике заболеваний, а также рациональному применению и назначению лекарственных средств;
- проведение индивидуальных консультаций с пациентами по их просьбе;
- наличие в аптеке информационных стендов о пропаганде здорового образа жизни;
- предоставление населению информационных брошюр и буклетов медико-санитарного содержания по вопросам здоровья.
6.5 Для представления медицинских консультаций по вопросам самолечения и профилактике заболеваний необходимо:
- наличие оборудованного места для проведения конфиденциальной беседы с пациентом;
- наличие в аптечной организации врача или соответственно обученного персонала;
- наличие стандартных операционных процедур (СОП) по надлежащему информированию пациентов;
- наличие необходимой справочной литературы, аудио-видеооборудования.
6.6 Информация, предоставляемая пациенту должна быть доступна к пониманию с учетом состояния пациента.
6.7 Для выполнения мероприятий, нацеленных на профилактику заболеваний и выявлению ранних симптомов, аптечной организацией может проводиться диагностическое тестирование. Выполнение диагностического тестирования пациентов (отдельных физиологических параметров: тестирование на беременность, на содержание сахара в крови, температуры тела, изменение артериального давления, веса, роста) осуществляет врач или соответственно обученный персонал.
Для этого необходимо:
- наличие соответствующего места/помещения для проведения тестирования;
- наличие стандартных операционных процедур (СОП) по проведению тестирования;
- наличие поверенного в установленном законом порядке оборудования, применяемого в процедурах проведения диагностического тестирования;
- поддержание связи фармацевта с лечащим врачом при длительном лечении пациента;
- соответствующая профессиональная подготовка фармацевта по предоставлению пациенту надлежащей консультации, включая направление к врачу, а также предоставление доврачебной помощи в случаях, когда это необходимо по результатам теста.
6.8 Все проводимые мероприятия необходимо документировать. Ответственность за хранение документации возлагается на лицо, ответственное за качество.
7 Обеспечение рационального применения рецептурных лекарственных препаратов
7.1 Обеспечение рационального применения рецептурных лекарств - деятельность, связанная с реализацией населению лекарственных препаратов, хранением, назначением и применением.
7.2 Деятельность персонала по обеспечению и рациональному применению лекарственных препаратов включает в себя:
- наличие достаточного количества квалифицированного персонала;
- соблюдение правил выписывания рецептов, технологии изготовления лекарственных форм, проверке соответствия прописанных доз возрасту больного, норм единовременного отпуска, совместимость выписанных лекарственных препаратов; [14, 15 ]
- соблюдение технологии изготовления и обеспечение качества лекарственных препаратов; [15, 16 ]
- осуществление отпуска рецептурных препаратов по рецептурным бланкам установленного образца;
- возможность приобретения пациентом выписанного лекарственного препарата в соответствующие сроки и по доступной цене;
- обеспечение надлежащего отпуска лекарственного препарата с соответствующей маркировкой и упаковкой;
- предоставление пациенту объективной информации о лекарственных препаратах доступными понятиями и советы по их применению.
7.3 Для обеспечения комплекса мероприятий, направленных на обеспечение рационального назначения и применения лекарственных препаратов фармацевту необходимо:
- соответствующие знания и навыки по предоставлению достоверной информации и консультативной помощи по применению лекарственных препаратов;
- систематическое повышение уровня знаний в области фармакотерапии, информации о новых лекарственных средствах, психологии общения;
- достаточное количество справочно-информационной литературы по использованию лекарственного препарата;
- взаимное сотрудничество с врачами;
- обратная связь с врачами в отношении прописывания лекарственных препаратов.
8. Влияние на назначение и использование лекарственных препаратов
8.1 Аптечная организация осуществляет деятельность, связанную с оказанием влияния на назначение и использование лекарственных средств и направленную на сотрудничество врача и фармацевта в системе обеспечения качества фармакотерапии пациенту.
8.2 Сотрудничество врача и фармацевта направлено на:
- назначение врачом лекарственных средств, включая правильность оформления и полноту сведений в рецепте;
- выписывание рецептов в соответствии с установленными правилами; [14 ]
- разработку схемы фармакотерапии;
- контроль за течением и результатами фармакотерапии;
- оценку данных по использованию лекарственных средств в медицинской и фармацевтической практике;
- оценку и предложения по эффективности рекламной информации о лекарственных средствах;
- использование специальных образовательных программ для специалистов здравоохранения;
- наличие справочных изданий, доступных для фармацевта и врача;
- обеспечение конфиденциальности данных, касающихся пациентов.
8.3 Основной формой сотрудничества врача и фармацевта является совместная разработка программ для реализации целей:
- по выбору лекарственных средств;
- по рациональной фармакотерапии;
- по мониторингу фармакотерапии.
8.4 Критериями выбора лекарственных средств для пациента являются следующие потребительские свойства:
- удобство и комфортность приема.
8.5 Фармацевт должен предоставлять врачу информацию об имеющимся ассортименте лекарственных препаратов на рынке, в данной аптечной организации, о ценах, свойствах и другое.
8.6 Разработка фармакотерапевтической программы предусматривает формирование схемы лекарственного лечения с учетом возможных альтернатив, обусловленных возможным наличием противопоказаний, побочных действий, особенностями питания и другими условиями.
8.7 Работа по рациональному назначению и эффективному использованию лекарственных средств может отражаться в фармацевтическом досье пациента. Фармацевтическое досье оформляется и ведется только с письменного согласия пациента, при условии полной конфиденциальности и невозможности доступа к досье посторонних лиц.
8.8 Сотрудничество врача и фармацевта позволит улучшить качество фармакотерапии, уменьшить число врачебных и фармацевтических ошибок, упорядочить информацию о побочных действиях лекарственных средств.
8.9 Допустимыми формами сотрудничества являются также: обсуждение вариантов корректировки фармакотерапии, совместное проведение фармакоэкономического анализа, участие в работе совещаний, конференций, терапевтических комиссий, формулярных комитетах.
8.10 Руководителем аптечной организации должно быть назначено ответственное лицо за организацию и проведение мониторинга побочных действий лекарственных средств.
8.11 В каждой аптечной организации должны быть карты - сообщений для заполнения их фармацевтами или пациентами после выявления побочных действий лекарственных средств.
Карта-сообщение заполняется самим пациентом или фармацевтом после получения информации о выявленном побочном действии лекарственных средств.
8.12 Данные карты-сообщений о выявленных побочных действиях лекарственных средств должны фиксироваться в журнале регистрации выявленных побочных действий лекарственных средств лицом, ответственным за мониторинг побочных действий лекарственных средств.
8.13 Сообщению подлежат все случаи выявления побочной реакции при осуществлении фармакотерапии.
8.14 Мониторинг побочных действий лекарственных средств осуществляется в соответствии с правилами, утвержденными уполномоченным органом в области здравоохранения. [17 ]
9.1 Деятельность связанная с самолечением направлена на консультирование пациента по самостоятельному приему лекарственных препаратов и предоставлении лекарственной помощи при лечении заболеваний и состояний, при которых возможно самостоятельное лечение.
9.2 Для осуществления деятельности, связанной с самолечением, фармацевту необходимо:
- соответствующая профессиональная подготовка по предоставлению пациенту надлежащих рекомендаций, включая направление к врачу в случаях, когда это необходимо;
- включение в программы обучения фармацевтов вопросов самолечения;
- участие в программах по выбору препаратов для самолечения и консультирования;
- наличие специальной справочной литературы;
- наличие перечня лекарственных препаратов, отпускаемых без рецепта;
- наличие стандартных операционных процедур (СОП) по вопросам самолечения;
- знание симптомов и недомоганий, излечивающихся самостоятельно;
- получение консультаций по вопросам самопомощи и самопрофилактики;
- наличие информационных материалов (брошюр, буклетов) для посетителей аптеки по самолечению.
9.3 Деятельность аптечной организации, связанная с самолечением состоит из следующих мероприятий:
- консультации пациента по применению безрецептурных лекарственных препаратов по просьбе или необходимости по самостоятельному приему лекарственных препаратов, направление к врачу, рекомендации по лекарственному взаимодействию с другими лекарственными препаратами и т.д.;
- консультации по использованию изделий медицинского назначения, предметов ухода, диагностических средств, средств для ухода за кожей, пищевых добавок, вспомогательных средств и устройств при самолечении;
- проведение фармацевтом оценки симптомов пациента о возможной принадлежности пациента к группе риска, наличие каких симптомов, продолжительности недомоганий, какие меры принимались при недомогании, при необходимости рекомендация безрецептурных лекарственных препаратов или направление к врачу;
- информировании врача о случаях возникновения осложнений при назначении безрецептурных лекарственных препаратов у конкретного пациента.
9.4 При рекомендации безрецептурных лекарственных средств фармацевт должен:
- использовать профессиональный опыт при выборе безрецептурных лекарственных препаратов с учетом их эффективности, безопасности и качества;
- доступно информировать пациента о данном препарате относительно его действия, способа применения, продолжительности лечения, возможных побочных действий, противопоказаний и сочетаемости с другими лекарственными средствами;
- предупредить пациента о необходимости обращения к врачу, в случае возникновения повторных симптомов.
10. Помещения и оборудование
10.1 Аптечные организации по характеру деятельности подразделяется на:
- аптеку с правом изготовления лекарственных препаратов, по рецептам врачей, по требованиям или заявкам медицинских организаций, организаций просвещения и социального обеспечения, стандартным прописям; внутриаптечной заготовки в соответствии с утвержденными прописями; фасовки лекарственных средств и лекарственного растительного сырья, а также осуществляющие реализацию готовых лекарственных препаратов, в том числе гомеопатических препаратов, изделий медицинского назначения, других товаров аптечного ассортимента населению;
- аптеку готовых лекарственных препаратов, без права изготовления лекарственных препаратов, осуществляющую реализацию населению готовых лекарственных препаратов, в том числе гомеопатических препаратов, изделий медицинского назначения и товаров аптечного ассортимента;
- аптеку медицинской организации (больничная, межбольничная) с правом изготовления лекарственных препаратов и обеспечения лекарственными средствами по требованиям без права розничной реализации населению;
- аптечный пункт, осуществляющий реализацию населению готовых лекарственных препаратов, в том числе гомеопатических препаратов, изделий медицинского назначения и других товаров аптечного ассортимента.
10.2 Аптека розничной реализации подразделяется на:
- аптеку с правом изготовления лекарственных средств (далее по тексту аптека с правом изготовления);
- аптеку готовых лекарственных препаратов.
10.3 Аптека с правом изготовления должна иметь в своей структуре следующие отделы:
- отдел реализации лекарственных препаратов отпускаемых по рецептам врача;
- отдел реализации безрецептурных лекарственных препаратов;
- отдел реализации изделий медицинского назначения и товаров аптечного ассортимента разрешенных к отпуску из аптеки.
10.4 Аптека готовых лекарственных препаратов должна иметь в своей структуре следующие отделы:
- отдел реализации лекарственных препаратов отпускаемых по рецептам врача;
- отдел реализации безрецептурных лекарственных препаратов;
- отдел реализации изделий медицинского назначения и товаров аптечного ассортимента, разрешенных к отпуску из аптеки.
10.5 Разрешается совмещать отдел реализации безрецептурных лекарственных препаратов с отделом реализации изделий медицинского назначения и товаров аптечного ассортимента, разрешенных к отпуску из аптеки.
10.6 Аптечная организация должна располагать необходимыми помещениями, оборудованием и инвентарем, обеспечивающие сохранение качества и безопасности лекарственных средств, изделий медицинского назначения при их хранении и реализации в соответствии с квалификационными требованиями.
10.7 Все помещения аптечной организации должны быть расположены в здании (строении) и функционально объединены в единый блок, изолированный от других организаций с отдельным входом (выходом).
Аптечной организации следует предусмотреть возможность входа (выхода) людям с нарушениями функций опорно-двигательного аппарата.
10.8 На площадях аптечных организаций не допускается размещение подразделений, функционально не связанных с указанными в лицензиях видами деятельности.
10.9 Аптечная организация должна иметь вывеску с указанием вида аптечной организации (в соответствии с лицензией на фармацевтическую деятельность) на государственном и русском языках, указанием организационно-правовой формы (в соответствии с правоустанавливающими документами), фирменного наименования организации, а также информацию о телефонах дежурных аптек.
10.10 Состав, размеры помещений и оборудование аптечной организации должны соответствовать объему и характеру осуществляемой фармацевтической деятельности и действующим нормативам, обеспечивающим качество и безопасность лекарственных средств и товаров аптечного ассортимента. [8, 13, 25 ]
10.11 Аптечные организации должны иметь системы электроснабжения, отопления, водоснабжения, кондиционирования, вентиляции, канализации.
10.12 Общая площадь административно-бытовых помещений аптечных организаций зависит от численности персонала и должна соответствовать действующим нормам и правилам. [8, 13, 25]
10.13 Все приборы, аппараты, используемые в аптечной организации, должны иметь технические паспорта, сохраняющиеся в течение всего времени эксплуатации. Необходимо регулярно проводить поверку приборов, аппаратов, в соответствии с требованиями нормативных документов, СТ РК 2.4 . [18 ]
10.14 Помещения хранения лекарственных препаратов, изделий медицинского назначения и товаров аптечного ассортимента должны быть оснащены приборами для регистрации параметров воздуха (термометрами, гигрометрами или психрометрами). Контролирующие приборы должны быть проверены в соответствии с СТ РК 2.4.
11. Прием, хранение и реализация
11.1 В аптечной организации должно быть предусмотрено отдельное помещение или специально оборудованное рабочее место, предусмотренное для приемки товара, обеспечивающее сохранение его качества и количества и не допускающее порчи и смешения с другой однородной продукцией.
11.2 Аптечная организация должна получать лекарственные препараты из организации, имеющей лицензию на оптовую реализацию.
11.3 Приемка лекарственных препаратов, изделий медицинского назначения и товаров аптечного ассортимента производится по количеству, качеству, комплектности и включает следующие этапы:
- проверка сопроводительной документации, характеризующей партию продукции (товаротранспортная накладная, счет-фактура, документ подтверждающий качество продукции - сертификат соответствия, санитарно-гигиеническое заключение);
- проверку соответствия серии лекарственного средства с серией указанной в сопроводительной документации;
- визуальную проверку поступившей продукции (бой, брак);
- проверку на соответствие маркировки, упаковки действующему законодательству Республики Казахстан;
- проверку соблюдения условий транспортирования.
11.4 Результаты приема продукции документируются.
11.5 В случае сомнения в качестве лекарственных средств, несоответствия серий, указанных в сопроводительных документах, несоответствия комплектности, упаковки, маркировки или недостачи по количеству, ответственное лицо за приемку продукции составляет претензию оптовой организации в соответствии с законодательством Республики Казахстан. [19, 20, 21 ]
11.6 Не подлежат приемке лекарственные средства, изделия медицинского назначения и товары аптечного ассортимента, с истекшим сроком годности, а также не соответствующие установленным требованиям к их качеству.
11.7 Лекарственные препараты, не прошедшие процедуру приема (при повреждении упаковки, не имеющие документа, подтверждающего качество, и/или необходимой сопроводительной документации) должны быть соответствующим образом промаркированы и размещены отдельно от других лекарственных средств до их идентификации, возврату поставщику или уничтожению в установленном законодательством порядке и иметь сигнальный ярлык: «На ответственном хранении. Хранить до принятия решения».
11.8 После проведения процедуры приемки, продукция приходуется и разрешается к реализации.
11.9 Лекарственные препараты, изделия медицинского назначения и товары аптечного ассортимента должны храниться в условиях, обеспечивающих сохранение их безопасности и качества в соответствии с нормативными документами, утвержденными государственным органом. [22 ]
11.10 В аптечной организации должны быть предусмотрены меры по исключению случаев хищения, повреждения (разливания, рассыпания, боя) и их контаминации.
11.11 При отпуске лекарственного препарата по рецепту врача фармацевт проводит оценку его соответствия установленным требованиям выписывания и таксирует его на отпускаемый лекарственный препарат. [14 ]
11.12 Замена, выписанного в рецепте лекарственного средства на его синоним (генерическую форму), производится с согласия пациента и/или по согласованию с врачом, при этом на обороте рецепта следует указать торговое наименование отпущенного лекарственного средства, поставить подпись и дату отпуска.
11.13 Аптечные организации обязаны отпускать лекарственные средства только в готовом для употребления виде и количествах, необходимых для выполнения врачебных назначений.
11.14 Лекарственное средство должно отпускаться в оригинальной заводской или аптечной упаковке. При необходимости допускается нарушение оригинальной заводской упаковки, за исключением блистерной, с обязательным указанием на аптечной упаковке наименования лекарства, количества, дозировки, серии, срока годности препарата, способа применения, мер предосторожности.
11.15 Аптечным организациям запрещается принимать от физических лиц лекарственные средства, приобретенные ими ранее.
11.16 Реализуемые из аптечных организаций лекарственные препараты должны иметь инструкцию по применению (аннотацию-вкладыш) на государственном и реализуемые русском языках, утвержденную государственным органом средства измерений медицинского назначения должны иметь сведения о их поверке, в виде оттиска клейма или сертификатов (свидетельств) о поверке. [4 ]
11.17 Пациенту по его просьбе может быть представлена дополнительная информация о приобретаемом лекарственном препарате, об имеющихся в аптечной организации синонимах (генерических формах), аналогах и их ценах.
11.18 При отпуске лекарственных препаратов фармацевт должен информировать пациента о правилах приема лекарственного препарата: режиме приема, разовой и суточной дозе, способе приема (с учетом приема пищи и пр.), правилах хранения, обращает внимание пациента на необходимость внимательного ознакомления с инструкцией по его применению. При отпуске средств измерений медицинского назначения фармацевт должен информировать пациента о правилах применения. Ответы специалиста должны быть аргументированными, грамотными, с соблюдением требований профессиональной этики.
12.1 Для выполнения основных функций штат аптечной организации должен быть укомплектован достаточным количеством квалифицированного персонала, способного на должном уровне решать профессиональные задачи в соответствии со своими должностными обязанностями, в случае применения приборов назначается ответственное лицо за состояние средств измерений.
Персонал аптечной организации должен соответствовать квалификационным требованиям в соответствии с требованиями законодательства Республики Казахстан. [8, 13, 25 ]
12.2 Ответственное лицо за качество, должно иметь высшее фармацевтическое образование и практический опыт работы.
12.3 Ответственное лицо за качество лекарственных средств, изготовляемых в аптеке, а также поступающих из аптечного склада, должно с целью предупреждения поступления в аптечную организацию некачественных лекарственных средств и недопущения снижения их качества в процессе хранения, обработки и отпуска, проводить мероприятия по обеспечению качества лекарственных средств, которые заключаются в проведении предупредительных мероприятий, осуществлении приемочного контроля, сертификации продукции.
Предупредительные мероприятия заключаются в:
- соблюдении санитарно-эпидемиологических правил и норм дезинфекционного и, противоэпидемического режимов;
- соблюдении правил и сроков хранения лекарственных средств;
- обеспечении исправности и точности весо-измерительных приборов;
- соблюдении врачами правил выписывания рецептов;
- соблюдении технологии изготовления лекарственных форм, соответствия прописанных доз, норм единовременного отпуска и другое;
- учете лекарственных средств с ограниченным сроком годности.
Приемочный контроль заключается в идентификации лекарственных средств по показателям «Упаковка», «Маркировка», «Описание» в соответствии с действующими нормативными документами.
12.4 В своей производственной деятельности специалист аптечной организации должен руководствоваться действующими нормативными правовыми актами в области здравоохранения, правилами внутреннего трудового распорядка, требованиями санитарно-эпидемиологических правил и норм, охраны труда, техники безопасности, должностными инструкциями, настоящим стандартом и иметь соответствующие полномочия для их выполнения.
12.5 Все сотрудники обязаны знать и выполнять принципы и правила надлежащей аптечной практики, проходить последующее повышение квалификации в соответствии с его должностными обязанностями.
12.6 В процессе своей деятельности специалисты аптечной организации обязаны соблюдать нормы фармацевтической этики и деонтологии.
12.7 Персонал аптечной организации, независимо от форм собственности, должен проходить аттестацию на профессиональную компетентность в порядке, установленном законодательством Республики Казахстан. [23 ]
12.8 Все сотрудники должны быть обеспечены достаточным количеством специальной одежды и обуви, проходить медицинское обследование в соответствии с установленным законодательством порядке. [13, 24, 25 ]
13. Стандартные операционные процедуры (СОП)
13.1 На все виды работ, влияющих на качество лекарственных средств, изделий медицинского назначения, а также качество деятельности аптечной организации в целом, должны быть составлены стандартные операционные процедуры (СОП).
13.2 СОП должны быть разработаны на: получение и проверку поставок продукции, безопасное хранение лекарственных средств, изделий медицинского назначения и товаров аптечного ассортимента, очистку (обработку) оборудования и уборку помещений (включая борьбу с паразитами), регистрацию параметров условий хранения, применения и содержания применяемых средств измерений, ведение и хранение документов, в том числе документов учета лекарственных препаратов, заказов, возврата, фармацевтического досье, документов мониторинга побочных действий, проведение обучения персонала.
13.3 СОП должны быть датированы и подписаны лицом, ответственным за качество и утверждены руководителем аптечной организации.
14.1 Форма и содержание документации, в зависимости от ее категории и вида, регламентируется руководителем организации и действующим законодательством Республики Казахстан.
14.2 Хранение документов осуществляется на бумажных и/или на электронных (магнитных) носителях.
14.3 Система документации аптечной организации должна обеспечивать:
- полную регламентацию выполняемых функций аптечной организации;
- доступность к соответствующей документации сотрудниками;
- однозначное толкование требований, изложенных в документах;
- своевременный пересмотр документации аптечной организации.
14.4 Документы должны быть доступны государственным органам для проверок в течение сроков, установленных действующим законодательством Республики Казахстан. Документация представляется по запросу государственного органа в полном объеме.
14.5 Документы должны храниться в условиях, обеспечивающих их сохранность, в течение срока, установленного законодательством Республики Казахстан.
15.1 Аптечной организацией должны регулярно проводиться самоинспекции (внутренние проверки) на соответствие требованиям действующего законодательства Республики Казахстан и настоящего стандарта.
15.2 Самоинспекция проводится с целью выявления недостатков по выполнению требований действующего законодательства по фармацевтической деятельности и надлежащей аптечной практики и вынесения рекомендаций проведения корректирующих действий.
15.3 Самоинспекция проводится лицом или независимой группой из числа сотрудников данной аптечной организации, независимыми от лиц, непосредственно осуществляющих проверяемую деятельность. В обязанности группы входят объективная оценка выполнения требований надлежащей аптечной практики, действующего законодательства и контроль за осуществлением корректирующих действий.
15.4 Программа по самоинспекции разрабатывается в виде СОП, обеспечивающих минимальные и единообразные типовые требования, охватывающие следующие пункты:
- помещения, включая помещения для персонала;
- содержание зданий и обслуживание оборудования;
- санитарно- эпидемиологические требования;
- техника безопасности и охрана труда;
- результаты предыдущих самоинспекций и предпринятых корректирующих действий.
15.5 После завершения самоинспекции должен быть составлен отчет, содержащий результаты самоинспекции, оценку и заключения, проведенные во время самоинспекции и при необходимости, рекомендации корректирующих действий и доводиться до сведения персонала, ответственного за проверяемый участок работы и руководства аптечной организации.
15.6 При последующих проверках контролируется выполнение рекомендаций и их эффективность.