






 Рейтинг: 4.6/5.0 (1896 проголосовавших)
Рейтинг: 4.6/5.0 (1896 проголосовавших)Категория: Бланки/Образцы
Данная информация не может использоваться при самолечении!
Обязательно необходима консультация со специалистом!
Что такое анаэробная микрофлора?
Анаэробная микрофлора – это микроорганизмы, для жизнедеятельности и размножения которых не нужен кислород. Для большинства из них он, наоборот, является губительным. Анаэробы населяют организм человека в норме. Пищеварительный тракт, система органов дыхания, мочеполовая система являются естественными местами их обитания. При снижении иммунитета или травматических повреждениях происходит активация инфекции с развитием воспалительного процесса. Организм человека в этом случае сам для себя становится источником заражения (эндогенное инфицирование). Реже анаэробы попадают в организм извне. В последнем случае требуется достаточно серьёзное и глубокое вмешательство, создающее бескислородные условия: глубокая колотая рана, инфицированный аборт, проникающие ранения брюшной и грудной полости, введение спиц и протезов.
Какие заболевания вызывают анаэробные микроорганизмы?
Развиваясь в толще кожи, мягких тканей и мышц, анаэробы вызывают целлюлиты, абсцессы, миозиты, могут стать причиной язвенного поражения стоп при диабете. Газовая гангрена – наглядный пример анаэробной инфекции. Абсцессы брюшной полости, лёгкого, предстательной железы, эмпиема плевры могут возникать самостоятельно или как осложнение оперативных вмешательств на этих органах. Анаэробное инфицирование матки (клостридиальный эндометрит) может стать следствием нелегального асептического аборта.
Симптомы, позволяющие заподозрить анаэробную инфекцию кожи и мягких тканей: плотный отёк, газообразование (ощущение, что лопаются пузырьки воздуха под кожей при надавливании), воспаление гнилостное, запах зловонный.
Когда назначают посев материала на анаэробную флору с определением её чувствительности к антибиотикам?
Исследование чаще всего применяют в хирургии, так как основное лечение анаэробного воспаления – хирургическое. Задача хирурга – устранить источник воспаления (при абсцедировании) либо раскрыть рану, обеспечив доступ кислорода, губительного для анаэробов.
Посев материала или отделяемого проводят для дифференциальной диагностики анаэробной и аэробной инфекций, так как принципы их лечения абсолютно разные, а также в качестве контроля эффективности проведенного лечения. Анаэробные микроорганизмы обладают чувствительностью к достаточно узкому спектру антибактериальных препаратов, поэтому целесообразно проводить лекарственную терапию после определения чувствительности к антибиотикам.
Какой материал забирают для исследования?
Подготовку к исследованию определяет врач индивидуально для каждой локализации воспалительного процесса. При инфицировании мягких тканей и кожи специальной подготовки не требуется.
Проводят посевы на анаэробную флору отделяемого из ран и абсцессов, биоптатов тканей и мазков из уретры, аспиратов из полости матки. Исследуют содержимое желчного пузыря, внутрисуставную и плевральную жидкости, грудное молоко, мочу. Анаэробы могут высеваться в мазках со слизистой носа и зева, с конъюнктивы, в смывах из бронхов.
Материал должен быть доставлен в лабораторию в анаэробных условиях, для чего используют специальные контейнеры.
Как трактуют результаты?
В норме анаэробы в диагностически значимых количествах не высеваются. Посев может обнаружить следующих представителей анаэробной микрофлоры (возбудителей инфекции): клостридий, бактероидов, фузобактерий, пептострептококков, вейлонелл, актиномицетов, превотелл, порфиромонад, фузобактерий. Рациональную антибактериальную терапию подбирают посредством определения чувствительности к антибиотикам. Следует понимать, что в некоторых случаях лекарства не смогут заменить хирургического лечения, а станут быть лишь дополнением к нему.
© 2016 apreka.ru. vet.apreka.ru . Использование материалов разрешено с указанием ссылки на сайт. Все наименования торговых марок принадлежат их законным правообладателям.
Информация размещена на сайте только для ознакомления. Обязательно необходима консультация со специалистом.
Если вы нашли ошибку в тексте, некорректный отзыв или неправильную информацию в описании, то просим вас сообщать об этом администратору сайта.
Отзывы размещенные на данном сайте являются личным мнением лиц их написавших. Не занимайтесь самолечением!
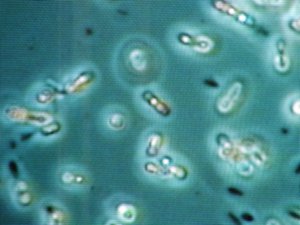 Бактерии присутствуют в нашем мире повсеместно. Они везде и всюду, и количество их разновидностей просто поражает.
Бактерии присутствуют в нашем мире повсеместно. Они везде и всюду, и количество их разновидностей просто поражает.
В зависимости от необходимости наличия кислорода в питательной среде для осуществления жизнедеятельности микроорганизмы классифицируют на следующие виды.
Термин «анаэробы» появился в 1861 году, благодаря работам Луи Пастера.
Анаэробные бактерии – это микроорганизмы, которые развиваются вне зависимости от присутствия в питательной среде кислорода. Они получают энергию путем субстратного фосфорилирования. Различают факультативные и облигатные аэробы, а также другие виды.
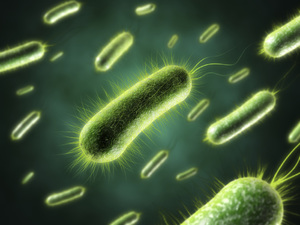 Факультативные бактерии могут существовать в любой среде. Причиной этого является то, что они могут менять один метаболический путь на другой. К ним причисляются кишечная палочка, стафилококки, шигеллы и другие.
Факультативные бактерии могут существовать в любой среде. Причиной этого является то, что они могут менять один метаболический путь на другой. К ним причисляются кишечная палочка, стафилококки, шигеллы и другие.Наиболее значимыми аэробами являются бактероиды. Примерно пятьдесят процентов всех гнойно-воспалительных процессов, возбудителями которых могут быть анаэробные бактерии, приходится на бактероиды.
Бактероиды – это род граммотрицательных облигатных анаэробных бактерий. Это палочки с биполярной окрашиваемостью, размер которых не превышает 0,5-1,5 на 15 мкм. Вырабатывают токсины и ферменты, которые могут вызывать вирулентность. Различные бактероиды обладают разной устойчивостью к антибиотикам: встречаются как устойчивые, так и чувствительные к антибиотикам.
Вырабатывание энергии в тканях человека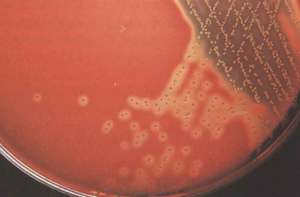 Некоторые ткани живых организмов обладают повышенной устойчивостью к пониженному содержанию кислорода. В стандартных условиях синтез аденозинтрифосфата идет аэробным путем, но при повышенных физических нагрузках и при воспалительных реакциях на первый план выходит анаэробный механизм.
Некоторые ткани живых организмов обладают повышенной устойчивостью к пониженному содержанию кислорода. В стандартных условиях синтез аденозинтрифосфата идет аэробным путем, но при повышенных физических нагрузках и при воспалительных реакциях на первый план выходит анаэробный механизм.
Аденозинтрифосфат (АТФ) – это кислота, играющая важную роль при вырабатывании организмом энергии. Существует несколько вариантов синтеза этого вещества: один аэробный и целых три анаэробных.
К анаэробным механизмам синтеза АТФ относятся:
Одной из задач микробиологии является культивирование анаэробных бактерий. Для выращивания многоклеточных анаэробных организмов требуется специальная микрофлора, а также определенные концентрации метаболитов. Применяется культивирование при различных исследованиях, например, при исследованиях паразитов, живущих в человеческом организме.
Существуют специальные методы для выращивания анаэробов. Они заключаются в замене воздуха на газовые смеси в герметизированных термостатах.
Другим способом будет выращивание микроорганизмов в питательной среде, в которую добавляют редуцирующие вещества.
Питательные среды для анаэробных организмов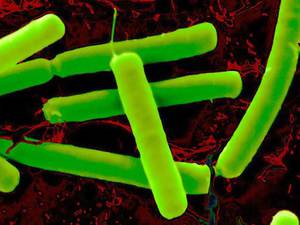 Существуют общие питательные среды и дифференциально-диагностические питательные среды. К общим относят среду Вильсона-Блера и среду Китта-Тароцци. К дифференциально-диагностическим – среды Гисса, среду Ресселя, среду Эндо, среду Плоскирева и висмут-сульфитный агар.
Существуют общие питательные среды и дифференциально-диагностические питательные среды. К общим относят среду Вильсона-Блера и среду Китта-Тароцци. К дифференциально-диагностическим – среды Гисса, среду Ресселя, среду Эндо, среду Плоскирева и висмут-сульфитный агар.
Базой для среды Вильсона-Блера является агар-агар с добавлением глюкозы, сульфита натрия и двухлористого железа. Черные колонии анаэробов образуются в основном в глубине агарового столбика.
Среда Ресселя (Рассела) используется в изучении биохимических свойств таких бактерий, как шигеллы и сальмонеллы. Она также содержит агар-агар и глюкозу.
Среда Плоскирева подавляет рост многих микроорганизмов, поэтому ее используют в дифференциально-диагностических целях. В такой среде хорошо развиваются возбудители брюшного тифа, дизентерии и другие патогенные бактерии.
Основное назначение висмут-сульфитного агара – выделение сальмонелл в чистом виде. Данная среда основывается на способности сальмонелл производить сероводород. Данная среда схожа со средой Вильсона-Блера по применяемой методике.
Анаэробные инфекцииБольшинство анаэробных бактерий, живущих в организме человека или животных, могут вызывать различные инфекции. Как правило, заражение происходит в период ослабления иммунитета или нарушения общей микрофлоры организма. Также существует вероятность попадания возбудителей инфекций из внешней среды, особенно поздней осенью и зимой.
Инфекции, вызванные анаэробными бактериями, как правило, связаны с флорой слизистых оболочек человека, то есть с основными местами обитания анаэробов. Как правило, у таких инфекций сразу несколько возбудителей (до 10).
Точное число заболеваний, вызванных анаэробами, практически невозможно определить в связи с затрудненным сбором материалов для анализа, транспортировкой образцов и культивированием самих бактерий. Чаще всего этот тип бактерий обнаруживают при хронических заболеваниях.
Анаэробным инфекциям подвержены люди любого возраста. При этом у детей уровень инфекционных заболеваний выше.
Анаэробные бактерии могут вызывать различные внутричерепные заболевания (менингит, абсцессы и другие). Распространение, как правило, происходит с током крови. При хронических заболеваниях анаэробы способны вызывать патологии в области головы и шеи: отит, лимфадениты, абсцессы. Несут опасность эти бактерии и желудочно-кишечному тракту, и легким. При различных заболеваниях мочеполовой женской системы также существует риск развития анаэробных инфекций. Различные заболевания суставов и кожи могут быть следствием развития анаэробных бактерий.
Причины появления анаэробных инфекций и их признаки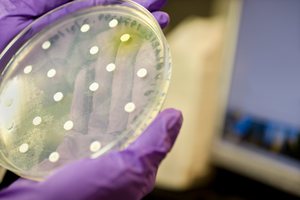 К возникновению инфекций приводят все процессы, во время которых на ткани попадают активные анаэробные бактерии. Также развитие инфекций могут вызвать нарушенное кровоснабжение и некроз тканей (различные травмы, опухоли, отеки, болезни сосудов). Инфекции ротовой полости, укусы животных, легочные заболевания, воспалительные заболевания тазовых органов и многие другие заболевания также могут быть вызваны именно анаэробами.
К возникновению инфекций приводят все процессы, во время которых на ткани попадают активные анаэробные бактерии. Также развитие инфекций могут вызвать нарушенное кровоснабжение и некроз тканей (различные травмы, опухоли, отеки, болезни сосудов). Инфекции ротовой полости, укусы животных, легочные заболевания, воспалительные заболевания тазовых органов и многие другие заболевания также могут быть вызваны именно анаэробами.
В разных организмах инфекция развивается по-разному. На это влияет и вид возбудителя, и состояние здоровья человека. Из-за трудностей, связанных с диагностированием анаэробных инфекций, заключение часто основывается на предположениях. Отличаются некоторыми особенностями инфекции, вызванные неклостридиальными анаэробами.
Первыми признаками заражения тканей аэробами являются нагноения, тромбофлебиты, газообразование. Некоторые опухоли и новообразования (кишечные, маточные и другие) также сопровождаются развитием анаэробных микроорганизмов. При анаэробных инфекциях может появляться неприятный запах, однако, его отсутствие не исключает анаэробов в качестве возбудителя инфекции.
Особенности получения и транспортировки образцовСамым первым исследованием в определении инфекций, вызванных анаэробами, является визуальный осмотр. Различные кожные поражения являются частым осложнением. Также свидетельством жизнедеятельности бактерий будет наличие газа в зараженных тканях.
Для лабораторных исследований и установления точного диагноза, прежде всего, надо грамотно получить образец материи из пораженного участка. Для этого используют специальную технику, благодаря которой нормальная флора не попадает в образцы. Наилучший метод – это аспирация прямой иглой. Получение лабораторного материала методом мазков не рекомендуется, но возможно.
К числу проб, непригодных для проведения дальнейшего анализа, относятся:
Для исследования могут быть использованы:
Транспортировать образцы необходимо максимально быстро в специальном контейнере или пластмассовой сумке с анаэробными условиями, так как даже кратковременное взаимодействие с кислородом может вызвать гибель бактерий. Жидкие образцы перевозят в пробирке или в шприцах. Тампоны с образцами транспортируют в пробирках с углекислым газом или заранее подготовленными средами.
Лечение анаэробной инфекции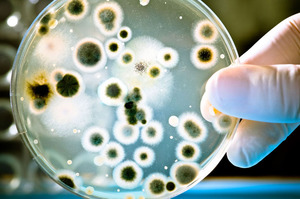 В случае диагностирования анаэробной инфекции для адекватного лечения необходимо следовать следующим принципам:
В случае диагностирования анаэробной инфекции для адекватного лечения необходимо следовать следующим принципам:
Для соблюдения этих принципов в лечении используют антибиотики, которые воздействуют как на анаэробов, так и на аэробные организмы, так как часто флора при анаэробных инфекциях носит смешанный характер. При этом, назначения лекарственные препараты, врач должен оценить качественный и количественный состав микрофлоры. К средствам, которые активны против анаэробных возбудителей относят: пенициллины, цефалоспорины, хлопамфеникол, фторхиноло, метранидазол, карбапенемы и другие. Некоторые препараты имеют ограниченное действие.
Для контроля среды обитания бактерий в большинстве случаев используют хирургическое вмешательство, которые выражается в обработке пораженных тканей, дренировании абсцессов, обеспечении нормальной циркуляции крови. Игнорировать хирургические методы не стоит из-за риска развития опасных для жизни осложнений.
Иногда используют вспомогательные методы лечения, а также из-за трудностей, связанных с точным определением возбудителя инфекции, применяют эмпирическое лечение.
При развитии анаэробных инфекций в ротовой полости также рекомендуется добавить в рацион как можно больше свежих фруктов и овощей. Наиболее полезны при этом яблоки и апельсины. Ограничению подвергают мясную пищу и фастфуд.
![]() Николаев Олег Петрович
Николаев Олег Петрович
Порой, общаясь с врачом, чувствуешь себя, как на чужой планете. Мозг получает кучу информации, которую он не понимает. Например, дисбактериоз, бифидобактерии, пробиотики, пребиотики. Да, эти слова на слуху, что-то из них для организма полезно, только вот что и почему? Вопрос может многих поставить в тупик. Молодые, заботливые мамы вообще при слове дисбактериоз впадают в панику и начинают заниматься самолечением, толком, не разобравшись, что это такое. И скорее всего, при таком лечении они только навредят ребёнку. Давайте попробуем разобраться в загадочном мире медицинских терминов.
Анаэробная микрофлора – это микроорганизмы, которым для роста и развития не нужен воздух. Например, стрептококки, стафилококки и другие.
Антагонизм – это борьба микроорганизмов за пищу и место.
Аэробная микрофлора – микроорганизмы, которым для роста и развития необходим воздух. Например, возбудитель туберкулёза и так далее.
Биоплёнка – это плёночка. которая покрывает поверхность эпителия кишечника. Состоит она из бактериального экзополисахарида. Биоплёнка является жильём для аутохотнной флоры (микроорганизмов, которые живут и размножаются в воде).
Гликокаликс – это слой оболочки клеток эпителия кишечника, образован он тонкими нитями. Состоит из олигосахаридов, связанных с кальциевыми мостиками.
Дисбактериоз – это изменение типичной микрофлоры, которые возникают из-за воздействия на микроорганизмы различными факторами. Такие изменения приводят к клиническими проявлениями со стороны макроорганизма, или изменения являются следствием патогенных процессов в организме человека. Этот дисбаланс приводит к снижению иммунитета, расстройству пищеварения, аллергическим реакциям и другим изменениям в организме. Чтобы справиться с дисбактериозом, необходимо выяснить причину, которая его вызвала, а попутно восстановить полезную микрофлору. Правильное лечение может назначить только врач. Возможно, вам помогут продукты (кефир, молоко и так далее). А возможно придётся обратиться за помощью к препаратам. Иногда врач прописывает препарат Нормобакт, в котором содержится огромное количество живых полезных бактерий и питательная среда, в которой эти бактерии могут расти и развиваться.
Дисбиоз – это дисбаланс полезной и патогенной микрофлоры организма, который проявляется в виде местных изменений, а впоследствии и общими нарушениями, из-за которых течение болезни отягощается.
Дисбактериоз кишечника – это нарушение в количественном и качественном составе микрофлоры кишечника.
Защитная микрофлора кишечника – микроорганизмы, которые помогают пищеварению, укрепляют иммунитет. Это бифидобактерии, лактобактерии, кишечная палочка.
Индигенная (резидентная, облигатная) флора – микроорганизмы, которые постоянно присутствуют в организме людей.
Колонизационная резистентность – объединение микроорганизмов, которые придают стабильность полезной микрофлоре, они обеспечивают защиту нашего организма от заселения чужеродных, патогенных микроорганизмов.
Комменсализм – это форма существования двух разных организмов, при которой один паразит. Это существование полезно для одного, а для другого абсолютно бесполезное.
М-микрофлора – это микроорганизмы, которые находятся в слизистой оболочке кишечника, они создают защиту: препятствуют проникновению через слизистую оболочку болезнетворных и условно-патогенных микроорганизмов (вызывают заболевание при определённых условиях). Также способствует нормальному течению обменных процессов.
Микробиоценоз – это совокупность микроорганизмов в определённом месте (кишечнике, полости рта и так далее), с одинаковыми потребностями.
Мутуализм – взаимовыгодное взаимодействие микрофлоры.
Нормальная флора – совокупность микроорганизмов в одном месте (кишечнике, носу и так далее), которое помогает организму нормально функционировать. Она представлена в организме бифидо-, лактобактериями и кишечной палочкой.
П-микрофлора (просветная) – микрофлора, которая находится в просвете кишечника. Например, вейлонеллы, бактероиды, энтеробактерии и другие.
Паразитизм – жизнедеятельность 2-х микроорганизмов, при котором, один выживает, только нанося вред другому.
Патогенная микрофлора кишечника – это флора, которая представлена патогенными микроорганизмами (сальмонеллами, стафилококками, клостридиями, иерсиниями, кишечными палочками и другими).
Пребиотики – это компоненты пищи, которые не усваиваются и не перевариваются в верхних отделах ЖКТ, а используются микрофлорой толстого отдела кишечника, стимулируют её рост и жизнедеятельность.
Пробиотики – пищевые продукты и препараты, которые содержат молочнокислые бактерии. Попав в организм, они помогают здоровью человека.
Сапрофитная микрофлора кишечника (паразитная) – микроорганизмы, для которых пищей являются конечные или промежуточные продукты жизнедеятельности макроорганизма (эпидермальный и сапрофитный стафилококк, дрожжи).
Симбиотоны – микроорганизмы разных видов, которые живут и питаются совместно.
Симбиоз – это тесное, взаимовыгодное и очень продолжительное существование представителей разных видов.
Синбиотики – это совокупность пребиотиков и пребиотиков. Опять возьмем за пример препарат Нормобакт. Его выпускают в порошке. В 1 саше препарата находится 4 миллиарда живых бактерий. Там же и находятся фруктоолигосахариды – это идеальная чреда, в которой растут и размножаются. Лактобактерии и бифидобактерии создают вокруг себя среду, в которой быстро погибают шиггелы, сальмонеллы, стрептококки, патогенные возбудители кишечной палочки и другие возбудители инфекций.
Условно-патогенная микрофлора кишечника – это микроорганизмы, которые при определенных условиях вызывают болезни у людей с пониженной сопротивляемостью. Эта флора представлена гемолитическим стрептококком, спороносными анаэробами, стафилококком, протеем.
Факультативная микрофлора – это временная флора, состав которой может поменяться.
Функциональные нарушения ЖКТ – нарушение работы пищеварительного тракта, изменение функций, изменение качественного и количественного состава микрофлоры, снижение иммунитета.
Функциональное питание – это продукты в рационе человека, которые нормализуют функции организма, улучшают общее состояние человека.
Эубиотики – это препараты, которые используют для нормализации микрофлоры кишечника.
Теперь, на приёме у врача вы не только сможете слышать медицинские термины, а будете понимать, что происходит у вас в организме.
1. Приказ Минздрава РФ от 09.06.2003 N 231 «ОБ УТВЕРЖДЕНИИ ОТРАСЛЕВОГО СТАНДАРТА «ПРОТОКОЛ ВЕДЕНИЯ БОЛЬНЫХ. ДИСБАКТЕРИОЗ КИШЕЧНИКА»
2. Смирнова Г.И. Ляликова В.Б. Методы диагностики и лечения дисбактериоза у детей / Первый Московский государственный медицинский университет им. М.И. Сеченова- М. 2012
3. Коровина Н.А. Захарова И.Н. и др, «Пребиотики и пробиотики при нарушениях кишечного микробиоценоза у детей»/Российская Медицинская академия последипломного образования МЗ РФ, 2004
Врач- терапевт Ланевская Рената Ивановна, 25 января 2013
Updated: 30.11.-0001 at 00:00
Анаэробы и аэробы – две формы существования организмов на земле. В статье речь идёт о микроорганизмах.
Анаэробы – микроорганизмы, которые развиваются и размножаются в среде, не содержащей свободный кислород. Анаэробные микроорганизмы обнаруживаются практически во всех тканях человека из гнойно-воспалительных очагов. Их относят к условно-патогенным (существуют у человека в номе и развиваются только у людей с ослабленной иммунной системой), но иногда они могут быть патогенными (болезнетворными). Различают факультативные и облигатные анаэробы. Факультативные анаэробы могут развиваться и размножаться и в бескислородной и в кислородной среде. Это такие микроорганизмы как кишечная палочка, иерсинии, стафилококки, стрептококки, шигеллы и другие бактерии. Облигатные анаэробы могут существовать только в бескислородной среде и погибают при появлении свободного кислорода в окружающей среде. Облигатные анаэробы подразделяют на две группы:
Клостридии — это возбудители анаэробных клостридиальных инфекций – ботулизма, клостридиальных раневых инфекций, столбняка. Неклостридиальные анаэробы это нормальная микрофлора человека и животных. К ним относят бактерии палочковидной и шаровидной формы: бактероиды, фузобактерии, пейллонеллы, пептококки, пептострептококки, пропионибактерии, эубактерии и другие. Но неклостридиальные анаэробы могут существенно способствовать развитию гнойно-воспалительных процессов (перитонит, абсцессы лёгких и головного мозга, пневмония, эмпиема плевры, флегмоны челюстно-лицевой области, сепсис, отит и другие). Большинство анаэробных инфекций, вызываемых неклостридиальными анаэробами, относятся к эндогенным (внутреннего происхождения, вызываемые внутренними причинами) и развиваются главным образом при снижении сопротивляемости организма, устойчивости к воздействию болезнетворных микроорганизмов в результате травм, операций, переохлаждения, снижения иммунитета.
Основную часть анаэробов, играющих роль в развитии инфекций составляют бактероиды, фузобактерии, пептострептококки и споровые палочки. Половину гнойно-воспалительных анаэробных инфекций вызывают бактероиды.
Клостридии – род спорообразующих анаэробных бактерий. Клостридии обитают на слизистых желудочно-кишечного тракта. Клостридии в основном патогенны (болезнетворны) для человека. Они выделяют специфические для каждого вида высокоактивные токсины. Возбудителем анаэробной инфекции может быть как один вид бактерий, так и несколько видов микроорганизмов: анаэробно-анаэробной (бактероиды и фузобактерии), анаэробно-аэробной (бактероиды и стафилококки, клостридии и стафилококки)
Аэробы — организмы, которым для жизнедеятельности и размножения необходим свободный кислород. В отличие от анаэробов у аэробов кислород участвует в процессе выработки необходимой им энергии. К аэробам относятся животные, растения и значительная часть микроорганизмов, среди которых выделяют.
Для каждого аэробного микроорганизма существует свой минимум, оптимум и максимум концентрации кислорода в окружающей его среде, необходимой для его нормального развития. Повышение содержания кислорода за границу «максимум» ведёт к гибели микробов. Все микроорганизмы гибнут при концентрации кислорода 40-50%.
Вам также может быть интересно
Здравствуйте! Подскажите пожалуйста что у меня не так в анализе. ПОСЕВ НА ФЛОРУ: рост микрофлоры в аэробных условиях не обнаружен! УРОГЕНИТАЛЬНЫЙ МАЗОК: Шейка матки: лейкоциты покрывают все п/з, эпителий плоский промежуточного слоя: 6-7 в п/зр эпителий цилиндрический. 6-8 в п/зр,местами группы до 25 эритроциты: умеренное количество гонококи: не обнаружены трихомонады: не обнаружены Влагалище: лейкоциты: 12-15 в п/зр эпителий плоский поверхностного слоя: значительное кол-во промежуточного слоя: значительное кол-во микрофлора: Гр(+) палочки обильно гонококки:не обнаружены трихомонады:не обнаружены Уретра: лейкоциты: единичные в п/зр эпителий плоский поверхностного слоя: 6-8 в п/зр микрофлора: ГР(+)палочки единчные гонококи:не обнаружены трихомонады:не обнаружены СПАСИБО.
Войти с помощью:
Войти с помощью:
Likar.Info в социальных сетях:
Внимание!
Информация, опубликованная на сайте, предназначена только для ознакомления. Описанные методы диагностики, лечения, рецепты народной медицины и т.д. самостоятельно использовать не рекомендуется. Обязательно проконсультируйтесь со специалистом, чтобы не нанести вред своему здоровью!
© likar.info 2001-2016. Торговая марка и торговый знак LIKAR.INFO™ зарегистрированы. Все права защищены. При использовании материалов сайта ссылка на www.likar.info обязательна.
danara Ученик (96), на голосовании 4 года назад
Голосование за лучший ответ
елена ващук Профи (680) 4 года назад
аэробы - это бактерии, которым для нормальной жизнедеятельности нужен кислород, в отличие от анаэробов. Обнаружить в моче флору можно только методом посева на питательные среды с последующей культивацией в условиях кислородной среды (вырастают аэробы если они есть). или в бескислородных ( растут анаэробы). То, что их не обнаружили - это хорошо.
Марья Кунникова Мастер (1208) 4 года назад
Аэробная микрофлора-живет только в кислородной среде, ну то есть там, где есть кислород. В принципе, если в моче нет микрофлоры (любой) -это хорошо.
МаргаритаФилатова Высший разум (124790) 4 года назад
Да! Хорошо! В мочевом пузыре в норме моча стерильна. Но при прохождении через нижнюю треть уретры происходит ее контаминация нормальной микрофлорой.
А выделяемые микроорганизмы: аэробы (стрептококки, стафилококки, энтеробактерии, неферментирующие, энтерококки), не обнаружены.

добрый день, мне 45 лет я рчень нуждаюсь в диагностике, прошу вас о помощи, после осмотра нефролога,уролога сданы анализы.
-Посев на флору и АЧ — В ДОСТАВЛЕННОМ ОБРАЗЦЕ РОСТ МИКРОФЛОРЫ В АЭРОБНЫХ УСЛОВИЯХ НЕ ОБНАРУЖЕН ;
-Глюкоза 6.0 ммоль/л 4.1 - 5.9 ммоль/л ;
-Посев на флору и АЧ — В ДОСТАВЛЕННОМ ОБРАЗЦЕ ЭТИОЛОГИЧЕСКИ ЗНАЧИМОЙ МИКРОФЛОРЫ НЕ ОБНАРУЖЕНО ;
-Микроскопия уретры Лейкоциты - 0-1-2 в п/зр.
Цилиндрический эпителий в умеренном количестве.
Эритроциты - 3-5 в п/зр.
Слизь в незначительном количестве.
Микрофлора - Гр (+) кокки, Гр(-) палочки - единично.
Гонококки, трихомонады - не обнаружено. ;
-Chlamydia trachomatis НЕ ОБНАР
Mycoplasma hominis НЕ ОБНАР
Ureaplasma ur.T-960 НЕ ОБНАР
Neisseria gonorrhoeae НЕ ОБНАР
Trichomonas vaginalis НЕ ОБНАР
Mycoplasma genitalium НЕ ОБНАР ;
-ПСА общий 0.227 нг/мл 0.0 - 4.0 нг/мл
ПСА свободный 0.111 нг/мл 0.00 - 0.42 нг/мл ;
беспокоит частые позывы к мочеиспусканию, и дискомфорт в уретре еще после опорожнения мочевого пузыря (УЗИ сделано с учетом опорожнения) остаеться ощущение потребности вновь мочиться и небольшая часть мочи попадает на белье, чего ранее не было. прошу вас. помогите мне правильно определить специалиста к которому следует обратиться. на сегодняшний день пропил курс Аугментина + канефрон + линекс +курантил.назначение нефролога. потом через 3 недели повтор анализов и курс норфлоксацина + уротол назначение уролога по прежнему результата нет. искренно с благодарностью за уделенное время и заботу.
 Глебов Антон Сергеевич
Глебов Антон Сергеевич
Выполните микроскопическое исследование на микрофлору секрета предстательной железы
0 Да Вы считаете ответ полезным?

Здравствуйте. у меня такой вопрос. мне 24 года в состоянии эрекции мой половой орган достигает 14см, у меня проблемы в половой жизни,с девушками совсем не общаюсь,скажите что можно сделать?Я Готов на крайние меры опирации итд. если можете скажите примерно сколько будет стоить итд.Только не нужно пожалуйста говорить о размерах итд полового органа т.к. я уже много читал и устал от этого меня не устраивает размер мой.
И где можно подойти в Днепр на консультацию к вам?

Здравствуйте. у меня такой вопрос. мне 24 года в состоянии эрекции мой половой орган достигает 14см, у меня проблемы в половой жизни,с девушками совсем не общаюсь,скажите что можно сделать?Я Готов на крайние меры опирации итд. если можете скажите примерно сколько будет стоить итд.Только не нужно пожалуйста говорить о размерах итд полового органа т.к. я уже много читал и устал от этого меня не устраивает размер мой.
И где можно подойти в Днепр на консультацию к вам?
проф. Кафарская Л.И. к.м.н. Ефимов Б.А. (РГМУ),
к.б.н. Артемова Л.В. к.б.н. Покровская М.С. (АО «ЛАГИС»)
В настоящее время, несмотря на широкое применение антибактериальных препаратов, инфекционные заболевания и осложнения в акушерстве и гинекологии, обусловленные микробными агентами, по-прежнему занимают доминирующее положение. Среди бактериальных заболеваний большой удельный вес составляют патологические состояния, связанные с нарушениями нормальной микрофлоры организма-хозяина, то есть с развитием вагинальных дисбактериозов. Частота возникновения таких заболеваний (бактериальный вагиноз, кандидозные вагиниты, атрофические вагиниты) не имеет тенденции к снижению. Дисбактериозы вагинального тракта могут явиться причиной развития патологических нарушений в других органах и системах организма женщины.
Микробиоценоз – это устойчивое сообщество микроорганизмов в определенной среде обитания. Факт существования микробиоценоза во влагалище, как и в кишечнике, установлен довольно давно. Однако изучение этого вопроса по-прежнему актуально – условия существования, состав микробиоценоза являются предметом научно-медицинских исследований. К чему приводят нарушения микробиоценоза, как поддержать или восстановить нарушенный микробиоценоз – вот вопросы, от которых во многом зависит здоровье человека.
Влагалище, вагинальная микрофлора и вагинальная среда, контролирующая микрофлору, образуют гармоничную, но весьма динамичную экосистему.
Вагинальная микрофлора включает в себя как микроорганизмы, формирующие нормальную микрофлору, так и случайно занесенные из окружающей среды бактерии (транзиторные микроорганизмы). Транзиторные микробы не способны к длительному пребыванию в генитальном тракте и, как правило, не вызывают развития патологических состояний до тех пор, пока факторы естественной резистентности и иммунные механизмы обеспечивают барьерную функцию и препятствуют избыточному размножению этих микроорганизмов.
Половые пути женщины представляют собой экологическую нишу, включающую в себя плоский эпителий влагалища, цилиндрический эпителий шейки матки и вагинальный секрет.
Вагинальный эпителий представляет собой сквамозный, многослойный эпителий, в базальном слое которого клетки делятся и созревают по направлению к просвету, затем слущиваются в просвет влагалища. Нормальное созревание эпителиоцитов, толщина поверхностного слоя и слущивание находятся под контролем гормонов яичников. В фолликулярной или пролиферативной фазе менструального цикла эпителий влагалища находится под воздействием эстрогенов (в основном эстрадиола), а в лютеиновой или секреторной фазе - прогестерона. Эстрогены индуцируют накопление в вагинальном эпителии гликогена, являющегося субстратом роста для лактобактерий. Лактобактерии расщепляют гликоген с образованием молочной кислоты, которая поддерживает рН влагалища на низком уровне (4,4-4,6). Кроме того, женские половые гормоны стимулируют образование рецепторов для лактобактерий на клетках вагинального эпителия (8).
При рождении влагалище новорожденной девочки стерильно, но уже в первые 24 часа колонизируется аэробными и факультативно-анаэробными микроорганизмами. В последующем, через несколько дней, в вагинальной микрофлоре новорожденной начинают преобладать лактобактерии. Это связано с наличием эстрогенов, полученных ребенком трансплацентарно от матери. Доминирование лактобактерий и ограниченность остальной флоры до кислотоустойчивых видов делает состав микрофлоры влагалища новорожденной девочки похожим на состав микрофлоры влагалища взрослых женщин.
К концу периода новорожденности трансплацентарно полученные эстрогены метаболизируются, происходит уменьшение запасов гликогена в эпителиоцитах и, как следствие, элиминация лактобактерий, среда становится менее кислой, в микрофлоре начинают доминировать анаэробы.
В пубертатный период, с началом овариальной функции, появляются эндогенные эстрогены, под влиянием которых в клетках вагинального эпителия вновь накапливается гликоген (“эстроген-стимулированный эпителий”) и повышается число рецепторов на клетках вагинального эпителия для лактобактерий. С этого времени лактобактерии начинают занимать доминирующее положение во влагалище и в последующем сохраняют это положение на протяжении всего репродуктивного периода у женщин (9).
У здоровых женщин детородного возраста состав вагинальной микрофлоры (см. следующий раздел) может изменяться в различные фазы менструального цикла, т.к. по циклу меняется уровень эстрогенов и, соответственно, гликогена в эпителиоцитах.
Во время беременности концентрация гликогена во влагалище у женщин увеличивается, что обеспечивает благоприятные условия для жизнедеятельности лактобактерий и повышения их уровня у беременных женщин. Максимальных значений количество лактобактерий достигает в III триместре беременности. Доминирование лактобактерий у беременных снижает риск контаминации плодных оболочек и развивающего плода, а также процесс патологической колонизации при прохождении его через родовые пути.
Роды приводят к резким изменениям состава микрофлоры влагалища. Снижается уровень лактобактерий и существенно увеличивается количество бактероидов, эшерихий. Эти изменения микрофлоры связаны со значительным снижением уровня эстрогенов, травмой родового канала, выделением лохий и способствуют развитию инфекционных послеродовых осложнений. Данные нарушения микробиоценоза временны, и к 6 неделе после родов состав микрофлоры возвращается к норме.
После наступления менопаузы в генитальном тракте снижаются уровни эстрогенов и гликогена, понижается окислительный потенциал, уменьшается количество лактобактерий, начинают преобладать облигатно-анаэробные бактерии, рН приобретает нейтральное значение (13).
Таким образом, существует ряд факторов женского организма, которые контролируют состав нормальной микрофлоры. Выраженные гормонозависимые изменения физиологии на протяжении жизни женщины, а также ежемесячные циклические изменения приводят к изменениям качественного и количественного состава вагинальной микрофлоры.
Микрофлора влагалища и ее значение в норме и патологии
Первое обширное исследование вагинальной микрофлоры у женщин было проведено Doderlein в конце 19 века. Doderlein и его современники считали, что вагинальная микрофлора состоит только из грамположительных бацилл.
Бациллы Додерляйна, известные в настоящее время как представители рода лактобактерий, являются преобладающими в нормальной микрофлоре женщин репродуктивного возраста (80-90%). При этом установлено, что нормальная вагинальная микрофлора весьма гетерогенна и включает в себя грамположительные и грамотрицательные аэробные, факультативно-анаэробные и облигатно анаэробные бактерии. Некоторые из этих микроорганизмов можно отнести к условно-патогенным. В норме их содержание во влагалище не превышает, как правило, концентрации 10? КОЕ/мл, и они не вызывают никаких патологий.
Грамположительные облигатно-анаэробные бактерииЛактобактерии - палочковидные бактерии, относятся к так называемой флоре Doderlein и занимают доминирующее положение во влагалище у здоровых женщин. В норме их уровень достигает концентрации 107-109 (иногда более) КОЕ/мл отделяемого влагалища. К типичным представителям лактофлоры относятся L. acidophilus, L. fermentum, L. plantarum и L. casei. По биохимическим свойствам лактобактерии относятся к облигатно-анаэробным бактериям. При этом они, как правило, устойчивы к кислороду (аэротолерантны).
Колонизируя эпителий влагалища, лактобактерии препятствуют контаминации вагинального тракта экзогенными микроорганизмами, и ограничивают излишний рост бактерий, постоянно присутствующих во влагалище, чрезмерное размножение которых может привести к возникновению патологических состояний (обеспечивают колонизационную резистентность). Важным фактором, необходимым для эффективной колонизации, является высокая способность лактобактерий к адгезии («прилипанию») на поверхности клеток вагинального эпителия. Причем различные штаммы лактобактерий обладают специфической адгезией к определенным эпителиоцитам. Так вагинальные штаммы лактобактерий проявляют высокий уровень адгезии только к вагинальному эпителию (кишечные – к эпителию кишечника).
Антибактериальная активность лактобактерий обусловлена рядом факторов. Прежде всего она связана с выработкой лактобактериями в процессе брожения молочной и других органических кислот, что обеспечивает низкое значение рН (кислая среда) во влагалище и является важнейшим контролирующим механизмом, препятствующим колонизации патогенными бактериями этой экологической ниши.
Вторым механизмом антагонистической активности лактобактерий является способность некоторых штаммов лактобактерий продуцировать перекись водорода. Лактобактерии, обладающие этим свойством, эффективно противостоят колонизации влагалища бактериями, которые играют наиболее важную роль при дисбиотических нарушениях микрофлоры влагалища.
Некоторые штаммы лактобактерий способны продуцировать и другие антибактериальные агенты, такие как лизоцим, лактацины и др.
В настоящее время доказано, что у здоровых женщин репродуктивного возраста лактобактерии доминируют не только во влагалище, но и в дистальных отделах уретры. Колонизируя уроэпителиальные клетки, лактобактерии предохраняют нижние отделы мочевыводящих путей от колонизации уропатогенными бактериями, способными вызывать восходящие урогенитальные заболевания. Во время менопаузы на фоне снижения уровня эстрогенов значительно возрастает частота возникновения пиелонефритов, циститов (10).
Бифидобактерии - наряду с лактобактериями относятся к флоре Doderlein, однако, по сравнению с последними, бактерии, принадлежащие к этому роду, выявляются, у здоровых женщин, с небольшой частотой равной 7-12 % (во время беременности выше 20 %) и в концентрациях варьирующих от 103 до 107 КОЕ/мл исследуемого материала. Как и лактобактерии, в процессе своей жизнедеятельности бифидобактерии выделяют большое количество кислых продуктов, тем самым, способствуя поддержанию во влагалище кислой среды (низкой рН).
Пептострептококки - являются третьей составляющей частью флоры Doderlein и относятся к представителям нормальной флоры генитального тракта. По различным данным частота их выделения в норме варьирует от 40 до 90 % случаев, а количество анаэробных кокков в вагинальном отделяемом составляет от 103 до 104 КОЕ/мл.
Несмотря на то, что пептострептококки составляют часть нормальной флоры женского полового тракта, их часто обнаруживают при септических абортах, трубно-яичниковых абсцессах, эндометритах и других тяжело протекающих инфекциях женских половых органов. В ассоциации с другими анаэробными бактериями пептострептококки в большом проценте случаев выделяют при бактериальном вагинозе, причем при этой патологии их количество может увеличиваться до 105 КОЕ/мл исследуемого материала или быть выше.
Клостридии - спорообразующие, палочковидные бактерии. Из влагалища здоровых женщин клостридии выделяются в небольших концентрациях и с низкой частотой (не превышающей 10% случаев). Роль этих микроорганизмов в микробиоценозе и в возникновении бактериального вагиноза невелика.
Пропионобактерии - относятся к представителям нормальной микрофлоры генитального тракта у женщин. Типичными представителями являются P. acnes, которые могут быть выделены с частотой до 25 % и в количестве, не превышающем в норме 104 КОЕ/мл исследуемого материала.
Мобилюнкусы - Грамм-вариабельные подвижные палочки. Бактерии этого рода могут обнаруживаться у женщин с диагнозами БВ, острый эндометрит, острый сальпингоофорит. Бактерии рода Mobiluncus выделяются только у 5 % здоровых женщин. У мужчин Mobiluncus могут вызывать острый уретрит и острый простатит. В случае длительного нелеченного заболевания возможно развитие серьёзного осложнения в виде эпидидимита или орхоэпидидимита, что может вызывать вторичное бесплодие.
Основное значение Mobiluncus приобретают у женщин с бактериальным вагинозом. Установлено, что у этой группы больных отмечается значительное увеличение концентрации этих бактерий на фоне снижения уровня вагинальных лактобактерий. При этом частота контаминации вагинального тракта данными микроорганизмами достигает от 30 до 50 % случаев, что позволяет рассматривать обнаружение этих бактерий как важный критерий для постановки диагноза дисбактериоза влагалища. В некоторых работах показано, что с развитием БВ связан только вид M. curtisii.
Представители рода Mobiluncus обладают способностью прикрепляться к эпителиоцитам влагалища. У бактерий этого рода были обнаружены муколитические ферменты: муциназа, нейраминидаза. Повышение активности этих ферментов в вагинальном секрете может приводить к разрыву плодных оболочек и преждевременным родам (11). Кроме этого показана роль Mobiluncus в развитии сальпингитов, эндометритов и абсцессов (17).
Atopobium vaginae - полиморфные кокки. Могут быть представлены в составе нормальной флоры мочеполовой системы у женщин. Cпособны продуцировать значительное количество аммиака, который может выступать как субстрат для микроорганизмов, вызывающих БВ, включая G.vaginalis (15). Atopobium vaginae играют роль в развитии БВ (ассоциированы на 95%). Кроме того вызывают воспалительные заболевания тазовых органов, инфекции мочеполовой и дыхательной систем. В настоящее время рассматривается влияние Atopobium vaginae на развитие анаэробных баланопоститов у мужчин. Клиническую значимость имеет встречающаяся резистентность Atopobium к метронидазолу (16).
Грамотрицательные облигатно-анаэробные бактерииГрамотрицательые строго анаэробные бактерии составляют значительную часть нормальной флоры ротовой полости, кишечного тракта и влагалища. Однако при определенных условиях эти бактерии могут вызывать сальпингиты, хориоамниониты, эндометриты и пельвиоперитониты. Эти же микроорганизмы в высоких концентрациях часто присутствуют при бактериальном вагинозе (5).
Бактероиды - неспорообразующие, полиморфные палочки. Наиболее часто встречающимся во влагалище видом является Bacteroides urealyticus, который выделяется у здоровых женщин с частотой до 36%. Бактероиды группы “fragilis” (B. fragilis, B. vulgatus, B. ovatus, B. distasonis, B. uniformis, B. caccae, B. multiacidus) могут быть обнаружены у 9-13% здоровых женщин. В норме количество бактероидов обычно не превышает 103-104 КОЕ/мл исследуемого материала. Могут быть представлены в составе нормальной флоры ЖКТ и дыхательной системы. Bacteroides играют роль в развитии БВ, вызывают воспалительные заболевания тазовых органов, пневмонии, инфекции ЖКТ.
Превотеллы - неспорообразующие палочки. Основными видами, наиболее часто встречающимися в вагинальном тракте здоровых женщин, являются P. bivia и P. disiens. В норме частота выделяемости бактерий этого рода может достигать 60% случаев, однако, их количественный уровень у здоровых женщин не превышает 104 КОЕ/мл исследуемого материала. Могут быть представлены в составе нормальной флоры ЖКТ и дыхательной системы. Prevotella играет роль в развитии у женщин БВ, вызывает такие инфекционные процессы как абсцессы, периодонтиты, бактериемии, пневмонии, остеомиелиты.
Порфиромонасы – неспорообразующие палочки. Типичными представителями этого рода, которые могут быть обнаружены в вагинальном секрете у здоровых женщин, являются бактерии, относящиеся к виду P. asaccharolitica, количественный уровень которых не превышает в норме 103 КОЕ/мл исследуемого материала. Частота встречаемости этих бактерий достигает 30% случаев.
Фузобактерии - неспорообразующие палочки. Являются представителями нормальной флоры ЖКТ. Фузобактерии в норме во влагалище встречаются наиболее редко (до 8% случаев) и в концентрации, не превышающей 103 КОЕ/мл исследуемого материала. При бактериальном вагинозе значительно возрастает частота выделения фузобактерий (21%). Они играют роль в развитии у женщин БВ (в основном Fusobacterium nucleatum), вызывают периодонтиты, гингивиты, бактериемии, амниониты.
Вейлонеллы – кокки, их количественный уровень в норме не превышает 103 КОЕ/мл исследуемого материала, а частота выделения 11%-14%.
Патогенные возможности строго анаэробных грамотрицательных бактерий, прежде всего, связаны с их ферментными системами. Так у B. fragilis выявлены гиалуронидаза, коллагеназа, фибринолизин, иммуноглобулин-протеазы, гепариназа и нейраминидаза. B. fragilis обладает и другими факторами патогенности, как, например капсульный полисахарид, обладающий антифагоцитарной активностью. Кроме того, бактероиды группы “fragilis” способны к продукции супероксиддисмутазы и каталазы, что позволяет им противостоять бактерицидному действию перекиси водорода, вырабатываемой лактобактериями. Различные протеазы и фибринолизин, выявлены у различных видов рода Prevotella и Porphyromonas. Fusobacterium necrophorum обладает гемолизином, лейкотоксином и факторами агрегации тромбоцитов.
У беременных женщин бактериальные протеазы и липазы могут воздействовать на хориоамниотическую мембрану, приводя к ее разрыву. Высокая продукция фосфолипазы А2 была определена у бактероидов, фузобактерий, а также у анаэробных стрептококков и G. vaginalis. Фосфолипаза А2 активирует продукцию простагландина путем освобождения арахидоновой кислоты из ее эфирной формы. Нарушение целостности хориоамниотической оболочки в совокупности с увеличением концентрации простагландинов в амниотической жидкости инициируют преждевременные роды.
Кислоты, продуцируемые грамотрицательными анаэробами, а также бактериями рода Mobiluncus, в частности янтарная кислота, ингибируют функциональную активность полинуклеарных нейтрофилов, с чем связывают их малое количество или отсутствие в выделениях из влагалища при бактериальных вагинозах.
Факультативно-анаэробные бактерииГарднереллы - плеоморфные грамотрицательные или грамвариабельные палочки или кокковидные палочки. В настоящее время известен единственный вид бактерий, принадлежащий к этому роду - Gardnerella vaginalis.
Гарднереллы встречаются у 50% сексуально активных женщин, причем их количество нередко достигает 105 КОЕ/мл исследуемого материала. При бактериальных вагинозах гарднереллы выделяются более чем в 90% случаев, в количестве превышающем 107 КОЕ/мл исследуемого материала и выше, и считаются важным фактором, ответственным за возникновение и поддержание этого патологического состояния.
G.vaginalis обладает выраженной способностью к адгезии на поверхности вагинальных эпителиоцитов. “Ключевые клетки” являются диагностическим признаком бактериальных вагинозов. Они представляют собой клетки сквамозного вагинального эпителия с обильно покрывающими их чаще всего G. vaginalis.
G.vaginalis могут продуцировать токсические биопродукты, к которым относятся муколитические ферменты и гемолизин. Существенное значение в формировании состояния бактериальных вагинозов отводится действию гемолизина G.vaginalis на человеческие лейкоциты. Симптомы бактериальных вагинозов проявляются на фоне недостаточности лейкоцитов. Предполагается, что G. vaginalis, которые присутствуют в высоких концентрациях у женщин с бактериальными вагинозами, продуцируют лейкотоксический фактор, способный разрушать лейкоциты, что позволяет объяснить отсутствие лейкоцитарной реакции при бактериальном вагинозе.
Микоплазмы - самые мелкие бактерии с выраженным полиморфизмом (от кокковидных телец до нитей), что обусловлено отсутствием ригидной клеточной стенки. Клинически доказана патогенность для человека Mycoplasma pneumoniae, Mycoplasma genitalium, Mycoplasma hominis, Ureaplasma urealyticum (по старой классификации – биовар Т-960), Ureaplasma parvum (по старой классификации – биовар Парво).
Ureaplasma urealyticum, Ureaplasma parvum и Mycoplasma hominis могут обитать в качестве коменсалов на слизистых урогенитального тракта. В норме Ureaplasma urealyticum/parvum выделяют у 6%-7% женщин в количестве 103 - 105 КОЕ/мл, Mycoplasma hominis у 2%-15% женщин в количестве до 103 КОЕ/мл исследуемого материала. Однако данные бактерии не могут рассматриваться как безвредные.
В том случае, если родовые пути матери контаминированы микоплазмами, слизистые оболочки ребенка могут быть колонизированы ими уже во время родов. Обычно в дальнейшем в первые недели жизни происходит прогрессивное исчезновение микоплазм. Тем не менее, известно, что пневмонии новорожденных нередко вызваны микоплазмами и уреаплазмами.
Контаминация Ureaplasma urealyticum/parvum половых путей женщины идет по восходящему пути. Наличие протеолитической активности в отношении IgA позволяет им преодолевать локальную защиту и благоприятствует их быстрой имплантации.
Доказана роль уреаплазм в возникновении негонококковых уретритов.
В патогенезе бактериального вагиноза основное значение придается только бактериям вида Mycoplasma hominis, частота выделения которых может увеличиваться до 50%-80%, а количественный уровень - до 105 КОЕ/мл и более исследуемого материала. При этой патологии микоплазмы всегда ассоциированы с другими бактериями и, прежде всего с облигатными анаэробами и гарднереллами.
Mycoplasma hominis, кроме того, может вызывать пиелонефриты и сальпингиты. В равной степени М. hominis и U. urealyticum/parvum могут быть ответственны за нарушения репродуктивной функции: бесплодие у мужчин, преждевременные выкидыши, хорио-амниониты, а также патологические неонатальные состояния: гипотрофия плода, преждевременный разрыв плодных оболочек.
Стафилококки. Грамположительные кокки. К видам, наиболее часто встречающимся во влагалище здоровых женщин, относятся коагулазо-негативные эпидермальные стафилококки (S. epidermidis), частота обнаружения которых может достигать 90% случаев, а количество варьировать от 103 до 104 КОЕ/мл исследуемого материала. Золотистые стафилококки (S. aureus) выделяются с небольшой частотой в 5% случаев и обычно колонизируют влагалище транзиторно. Золотистые стафилококки способны вырабатывать TSST-1 токсин, результатом действия которого является синдром токсического шока.
Стрептококки. Грамположительные кокки. В норме во влагалище здоровых женщин выделяют стрептококки в количестве не более, чем 103 КОЕ/мл, относящиеся в основном к трем группам: стрептококки группы viridans (“зеленящие” стрептококки или “?- (или ?-) гемолитические Streptococcus sp.), стрептококки серологической группы В (S. agalactiae) и стрептококки серологической группы D (энтерококки).
У новорожденных стрептококки группы В (S. agalactiae) способны вызывать тяжелые инфекционные состояния, включающие респираторные осложнения, менингиты, септицемии, нередко приводящие к смерти. Поэтому необходимо обследовать беременных на предмет присутствия во влагалище стрептококков группы В, а при выявлении таковых назначать антибактериальную терапию (стрептококки группы В обладают чувствительностью практически ко всем ?–лактамным антибиотикам).
Энтерококки являются нормальными представителями желудочно-кишечного тракта и урогенитального тракта человека. Однако бактерии этого рода очень часто обнаруживаются при воспалительных заболеваниях мочеполовой системы, а также могут вызывать инфекционные эндокардиты.
Зеленящие стрептококки часто являются причиной пост операционных воспалительных осложнений и являются основной причиной инфекционных эндокардитов.
Энтеробактерии. Грамотрицательные палочки. Наиболее часто встречающимся во влагалище здоровых женщин видом этой группы микроорганизмов являются Escherichia coli. Частота их выделения варьирует от 10% до 25%, а количество от 103 до 104 КОЕ/мл исследуемого материала. Другие виды бактерий семейства Enterobcteriaceae, например, принадлежащих к родам Klebsiella и Enterobacter, также могут быть выделены из влагалища здоровых женщин, однако значительно реже. Escherichia coli, Proteus sp. Klebsiella sp. а также Pseudomonas aeruginosa, могут вызывать урогенитальные инфекционные заболевания (неспецифические вагиниты и др.).
Дрожжеподобные грибы рода Candida являются частыми коменсалами генитального тракта здоровых женщин, особенно сексуально активных. Наиболее часто обнаруживаемым видом является Candida albicans (до 30%). Количество Candida albicans может достигать 106 КОЕ/мл исследуемого материала, при этом не вызывая развития патологических процессов. Количество дрожжеподобных грибов рода Candida может повышаться при беременности на фоне транзиторной физиологической супрессии клеточного иммунитета.
Этиология и патогенезБактериальный вагиноз (БВ) – наиболее широко распространенное заболевание у женщин детородного возраста. Это заболевание с полимикробной этиологией, в основе которого – нарушение нормального микробиоценоза влагалища. По сути БВ – это дисбактериоз влагалища. Выраженные нарушения в составе вагинальной микрофлоры при БВ являются фактором высокого риска возникновения эндометрита, сальпингоофорита, преждевременных и осложненных родов и абортов (1).
В настоящее время нет единой точки зрения на возможные пути передачи БВ, но известно, что БВ встречается прежде всего, у сексуально активных женщин. Вместе с тем, только одной передачи микроорганизмов не достаточно для возникновения бактериального вагиноза. Для развития заболевания необходимо наличие дополнительных факторов риска.
К предрасполагающим факторам, ведущим к развитию БВ следует отнести: применение антибиотиков, длительное использование внутриматочных контрацептивов, воспалительные заболевания половых органов, нарушения гормонального статуса, сопровождающиеся нарушением менструального цикла, преимущественно по типу олигоменореи или аменореи, изменение состояния местного иммунитета, стрессовые воздействия на организм, использование контрацептивных препаратов со спермицидной активностью, регулярные спринцевания, частая смена половых партнеров (1).
ДиагностикаДиагностика бактериального вагиноза состоит из совокупности клинических и лабораторных тестов (5).
Пациентки предъявляют жалобы на обильные выделения из половых путей с неприятным запахом, усиливающимся после полового акта. Иногда возможен зуд и дизурические явления.
Для диагностики БВ после гинекологического осмотра производится забор влагалищного отделяемого с заднего свода влагалища. Если обследование предполагает только качественное исследование, забор осуществляется двумя ватными тампонами, один из которых помещают в пробирку с транспортной средой, а другой используют для определения рН и приготовления мазка.
Предварительный диагноз БВ может быть поставлен в случае обнаружения следующих клинических признаков и результатов лабораторных исследований:
Диагноз БВ может быть поставлен лишь на основании наличия не менее 3-х из 4-х признаков (Amsel). Ни один из них в отдельности не имеет самостоятельного диагностического значения.
Подтверждением правильности предварительного диагноза является оценка количественного и качественного состава микрофлоры вагинального тракта пациентки, полученная в результате микробиологического исследования выделений из влагалища.
Микробиологическое исследование является наиболее достоверным этапом в диагностике БВ и служит критерием для оценки клинического значения скрининговых методов диагностики БВ. Однако до настоящего времени оно остается достаточно длительной и дорогостоящей процедурой. Анаэробы, ассоциированные с БВ, относятся к труднокультивируемым микроорганизмам, требующим специальных условий для роста на питательных средах. При наличии в образце персистирующих форм анаэробных бактерий, что встречается в последнее время все чаще, возможно получение ложноотрицательных результатов. Это связано с тем, что персистирующие бактерии не способны к росту на питательных средах, т.е. являются некультивируемыми формами.
В настоящее время для диагностики дисбактериозов влагалища активно используются и различные виды ПЦР-исследований.
«ПЦР в реальном времени» с количественным определением возбудителей – наиболее информативный, но также достаточно дорогой и малодоступный для широкого применения вариант исследования.
Лаборатория «ЛАГИС» предлагает оптимальный подход к лабораторной диагностике дисбактериозов – применение метода ПЦР с использованием тест-систем с заданной чувствительностью для выявления условно-патогенных анаэробных бактерий и полуколичественную тест-систему для определения лактобактерий.
Чувствительность ПЦР-тест-систем для выявления условно-патогенных анаэробов, ассоциированных с дисбактериозом влагалища - 10 4 КОЕ/мл и более (специфичность – близка к 100%). Использование таких тест-систем позволяет при положительном результате получать информацию о диагностически значимом количестве данных бактерий в образце.
В настоящее время кроме «традиционных» G. vaginalis, Mycoplasma hominis, Ureaplasma sp. Candida sp. к микроорганизмам, ассоциированным с дисбактериозом влагалища, относят и анаэробные бактерии родов Prevotella, Bacteroides, Mobiluncus, Fusobacterium, а также Atopobium vaginae и др.
Важное диагностическое значение для оценки микробиоценоза влагалища имеет установление концентрации лактобактерий во влагалище. Полуколичественная ПЦР-тест-система дает три варианта результата исследования пробы биоматериала:
Результат исследования (количество лактобактерий)
Как видно из представленных выше результатов, частота обнаружения этих микроорганизмов резко возрастает при совместном выявлении с G. vaginalis. Это свидетельствует о том, что при БВ часто выявляются условно-патогенные анаэробные бактерии, участвующие в патологическом процессе в концентрации более чем 104 кл/мл.
Таким образом, при диагностике дисбактериозов (БВ и др.) для определения состава микрофлоры влагалища, можно порекомендовать комплексное ПЦР -исследование мазка с заднего свода влагалища на условно-патогенные бактерии и нормофлору:
При необходимости можно расширить это исследование до патогенных микроорганизмов (хламидии, гонококки, трихомонады, микоплазмы гениталиум).
Помимо перечисленных ПЦР-исследований рекомендуется использовать следующие традиционные методы: проведение аминного теста, измерение рН вагинального секрета, микроскопию мазка (дает информацию о наличии ключевых клеток, лейкоцитозе и др.).
Актуальность лабораторной диагностики дисбактериоза влагалища не вызывает сомнений. Причем существуют индивидуальные особенности развития этих патологических состояний, зависящие от состава условно-патогенной микрофлоры. Эти особенности необходимо учитывать при выборе пути лечения для каждой пациентки.
ЛечениеЦелью проводимой терапии является элиминация условно патогенных микроорганизмов, нехарактерных для данного биотопа и восстановление нормальной микрофлоры влагалища.
Современное лечение бактериального вагиноза является двухэтапным.
На первом этапе используются антибактериальные препараты, обладающие антианаэробной активностью. К этой группе препаратов относится метронидазол, содержащий имидазоловое кольцо и обладающий выраженной активностью по отношению к неспорообразующим анаэробным бактериям, но не имеющий активности по отношению к гарднереллам. Подавляя рост и размножение неспорообразующих анаэробов метронидазол нарушает синергическое взаимодействие между анаэробами и гарднереллами, что проявляется положительным эффектом в лечении БВ.
Основным альтернативным препаратом в лечении БВ в настоящее время является клиндамицин. Пероральное применение клиндамицина может осложняться развитием псевдомембранозного колита. Учитывая, что наряду с высокой эффективностью при пероральном применении наблюдается большое количество нежелательных побочных реакций, клиницисты отдают предпочтение местному интравагинальному применению этих препаратов (3-х дневный курс лечения). Клиническая эффективность применения метронидазола и клиндамицина достигает 85-94%. К сожалению, клиндамицин не обладает селективным воздействием и наряду с элиминацией бактероидов, превотелл, гарднерелл оказывает негативное влияние и на лактобактерии. Дефицит лактобактерий, усугубляющийся после лечения антибактериальными препаратами служит предрасполагающим фактором для возникновения возвратных БВ. В этой связи, после проведения успешной антибиотикотерапии частота рецидивов БВ достигает 30%. Поэтому важной составной частью лечения БВ является использование препаратов-пробиотиков на втором этапе лечения.
В настоящее время для второго этапа лечения БВ применяются препараты-пробиотики: «Ацилакт», «Лактобактерин», «Бифидумбактерин». Они представляют собой лиофилизированную биомассу лакто- или бифидобактерий, выделенных из кишечника здоровых людей и применяются на тампонах или в виде свечей интравагинально.
В процессе жизнедеятельности вносимых лактобактерий снижается рН вагинального содержимого, возникает антагонистическая активность по отношению к условно патогенным микроорганизмам, стимулируется рост индигенной лактофлоры. Кроме того, в исследованиях последних лет подтвердили и противовоспалительный эффект пробиотиков. Использование препаратов-пробиотиков на втором этапе лечения БВ позволяет значительно снизить частоту рецидивов БВ.
Контроль леченияНаиболее информативным методом, позволяющим контролировать эффективность лечебных мероприятий, является полноценное микробиологическое исследование отделяемого с заднего свода влагалища (так же, как и для диагностики БВ). К сожалению, этот метод достаточно длительный в исполнении, дорогостоящий и дающий ложноотрицательные результаты в случае персистенции (некультивируемые формы).
Используя полуколичественное определение концентрации лактобактерий методом ПЦР (тест-система АО «ЛАГИС»), можно быстро и надежно контролировать эффективность лечения дисбиоза, так как восстановление микробиоценоза однозначно соответствует восстановлению уровня лактобактерий более 10 6 кл/мл.
Используя ПЦР-тест-системы АО «ЛАГИС» для выявления условно-патогенных анаэробов (см. выше) можно определить маркеры дисбиоза в диагностическом количестве (более 10 4 кл/мл).
В случае успешного лечения условно-патогенная флора не должна выявляться, так как количество этих бактерий должно уменьшиться до неопределяемого.
Список литературы